Neonatale tumoren komen elke 12.500 tot 27.500 levendgeborenen voor en vertegenwoordigen 2% van de maligniteiten bij kinderen. Mesoblastisch nefroma (ook wel foetaal nierhamartoom genoemd) is de meest voorkomende niertumor die in de neonatale periode wordt geïdentificeerd en de meest frequente goedaardige niertumor op kinderleeftijd. Hij vertegenwoordigt 3-10% van alle pediatrische niertumoren. Deze tumor werd voor het eerst beschreven als een afzonderlijke entiteit door Bolande et al in 1967. Voordien werd hij abusievelijk verward met de congenitale Wilms tumor.
De diagnose van mesoblastisch nefroma kan antenataal worden gesteld op echografie. Polyhydramnios wordt gerapporteerd in 71% van de zwangerschappen geassocieerd met mesoblastisch nefroma. De meest voorkomende klinische presentatie is een asymptomatische abdominale massa. Paraneoplastische syndromen zoals hypertensie of hypercalciëmie kunnen aanwezig zijn. Hypertensie wordt verondersteld secundair te zijn aan verhoogde renineproductie door de opgesloten glomeruli in de tumor. De differentiële diagnose omvat Wilms tumor.
De radiologische kenmerken van mesoblastisch nefroma worden getoond in de beelden hieronder.
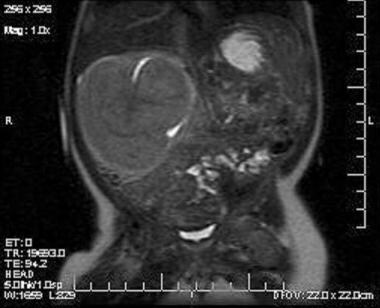 Coronale T2 opname toont een solide massa die ontstaat uit de bovenste pool van de rechter nier. Het normale nierweefsel is naar inferior verplaatst. Een deel van het nierbekken dat door de massa wordt ingesloten, verschijnt als een hyperdensiteit in de massa. De massa is isodens aan het nierparenchym op alle sequenties.
Coronale T2 opname toont een solide massa die ontstaat uit de bovenste pool van de rechter nier. Het normale nierweefsel is naar inferior verplaatst. Een deel van het nierbekken dat door de massa wordt ingesloten, verschijnt als een hyperdensiteit in de massa. De massa is isodens aan het nierparenchym op alle sequenties.  Coronale T1-opname door de massa die afkomstig is van de bovenste pool van de rechter nier. De massa is isodensse ten opzichte van de nier. Ze vertoont een homogeen signaal zonder centrale necrose of bloeding.
Coronale T1-opname door de massa die afkomstig is van de bovenste pool van de rechter nier. De massa is isodensse ten opzichte van de nier. Ze vertoont een homogeen signaal zonder centrale necrose of bloeding.  Axiale foto bij een 3 maanden oude zuigeling met een palpabele abdominale massa. Het beeld toont een grote, homogene, niet-verhogende vaste massa die uit de bovenpool van de rechternier komt. Het normale nierweefsel is inferieur oplichtend te zien. Uitscheiding van contrast in het bekken, ingesloten door de massa, is te zien als centrale hyperdensiteit in het centrum van de massa.
Axiale foto bij een 3 maanden oude zuigeling met een palpabele abdominale massa. Het beeld toont een grote, homogene, niet-verhogende vaste massa die uit de bovenpool van de rechternier komt. Het normale nierweefsel is inferieur oplichtend te zien. Uitscheiding van contrast in het bekken, ingesloten door de massa, is te zien als centrale hyperdensiteit in het centrum van de massa. Pathofysiologie
De klassieke variant presenteert zich meestal voor de leeftijd van 3 maanden als een solide massa met kleine necrose- of bloedingshaarden. Het dringt niet door in de perinefrische weefsels of de vasculaire pedikel. Het wordt geassocieerd met een uitstekend resultaat na volledige chirurgische resectie van de tumor. Op het eerste gezicht is de solide tumor niet ingekapseld, met een wervelvormig trabeculaat dat lijkt op leiomyomen – vandaar de naam leiomyomateus hamartoom van de nier. Histologisch bestaat het uit uniforme spindelcellen, gerangschikt in bundels met verspreide foci van ingesloten normale glomeruli en tubuli.
Het cellulaire type presenteert zich gewoonlijk na de leeftijd van 3 maanden en vertoont agressievere beeldvormingskenmerken, met grotere gebieden van necrose en bloeding. Het kan het perinefrisch vet en bindweefsel binnendringen. Het wordt geassocieerd met een hogere frequentie van lokaal recidief en metastatische ziekte. Bij macroscopisch onderzoek is het cellulaire type een vlezige tumor met meerdere foci van necrose, cystische verandering en bloeding. Histologisch bestaat de tumor uit spindelcellen, gerangschikt in lukrake bladen met een beperkte neiging tot bundelvorming, zoals bij de klassieke vorm.
Een frequente genetische verandering is de translocatie t(12;15) die resulteert in een fusie van het ETV6-gen op 12p13 en het NTRK3-gen op 15p15, die bijna uitsluitend voorkomt in de cellulaire variant, die diagnostisch is. Omgekeerde transcriptie polymerase kettingreactie (RT-PCR) kan de ETV6-NTRK3 genfusie aantonen, een kenmerk dat ook wordt gezien bij congenitaal infantiel fibrosarcoom – vandaar de naam infantiel fibrosarcoom van de nier.
Voorkeur voor onderzoek
De massa kan voor het eerst worden gediagnosticeerd wanneer de gedetailleerde scan van de foetale anatomie wordt verricht bij een zwangerschapsduur van 18-20 weken. Het onderscheid tussen een solide en een cysteuze massa kan gemakkelijk worden gemaakt op echografie om onderscheid te maken tussen een massa en hydronefrose. Als de massa erg groot is, kan het in sommige gevallen moeilijk zijn om het orgaan van oorsprong te bepalen. Magnetische resonantiebeeldvorming (MRI) van de foetus kan nuttig zijn om het orgaan van oorsprong te bepalen, omdat MRI een uitstekende detaillering van de weke delen biedt en beeldvorming in meerdere vlakken mogelijk is. Beweging van de foetus kan de MRI-beelden echter beperken.
Postnataal is echografie gewoonlijk het eerste beeldvormende onderzoek dat wordt uitgevoerd wanneer de abdominale massa wordt gepalpeerd. Ultrasonografie is gemakkelijk en op grote schaal beschikbaar, is niet duur en er komt geen ioniserende straling aan te pas. Alle transversale beeldvormende onderzoeken, zoals ultrasonografie, computertomografie (CT) en MRI, kunnen helpen bij het bepalen van het orgaan van oorsprong en de relatie tot de ipsilaterale nier. MRI is echter de meest nauwkeurige beeldvormingsmodaliteit voor het afbeelden van de lokale en regionale omvang van de tumor. Dit komt door het vermogen van MRI om de anatomie in verschillende vlakken zeer gedetailleerd weer te geven.
In een studie van 30 kinderen (15 jongens, 15 meisjes) met congenitaal mesoblastisch nefroma, vonden Chaudry et al dat cystische componenten gemakkelijk werden geïdentificeerd op ultrasonografie (US), centrale bloeding gemakkelijk werd geïdentificeerd op CT-scanning, en MRI was zeer gevoelig voor cystische componenten en centrale bloeding. De auteurs merkten op dat bevindingen die wijzen op de klassieke variant een perifere hypoechoische ring of een grote vaste component omvatten, terwijl cystische/necrotische verandering en bloeding vaker voorkwamen in de cellulaire variant.
Beperkingen van technieken
Imaging bevindingen kunnen de diagnose prenataal of na de geboorte suggereren, en ze kunnen worden gebruikt om het orgaan van oorsprong te identificeren. Zij kunnen een waarschijnlijke of meest waarschijnlijke diagnose suggereren op basis van de beeldvormingskenmerken. Beeldvormingsresultaten kunnen echter niet worden gebruikt om een mesoblastisch nefroma definitief te onderscheiden van een congenitale Wilms tumor. Histologisch onderzoek is de enige definitieve test.
Ultrasonografie is ruim beschikbaar en wordt routinematig antenataal uitgevoerd. Het heeft echter het nadeel dat het de meest operator-afhankelijke modaliteit is. Het is mogelijk dat de tumorranden niet nauwkeurig kunnen worden gevisualiseerd, vooral bij grote tumoren. Bij grote tumoren is het ook mogelijk dat het orgaan van oorsprong niet definitief kan worden bepaald.
CT-scanning is niet nuttig als prenatale beeldvormingsmodaliteit vanwege de blootstelling aan ioniserende straling en het gebruik van intraveneus contrast. Postnataal bestaan dezelfde nadelen. Bovendien kan een nauwkeurige vertraging na contrastinjectie moeilijk te bepalen zijn vanwege het kleine contrastvolume dat bij pasgeborenen wordt gebruikt. Het contrast van de weke delen is in deze leeftijdsgroep ook beperkt, door het ontbreken van peritoneaal vet. Bij oudere patiënten zou CT ook sedatie vereisen.
MRI wordt steeds meer gebruikt als prenataal diagnostisch hulpmiddel. Prenataal MRI-onderzoek kan worden beperkt door beweging van de foetus en ongemak bij de moeder. Bovendien kan voor MRI sedatie nodig zijn, aangezien de typische onderzoekstijden langer zijn. Intraveneus contrast kan nodig zijn om de tumor volledig te karakteriseren.