A ptosis, hivatalos nevén blepharoptosis, egy gyakori lelet, amelyet a felső szemhéj lógása jellemez elsődleges tekintet esetén. Általában a ptosis csupán az öregedés velejárója, de egyes előfordulások szisztémás betegségekkel vagy genetikai rendellenességekkel állnak összefüggésben. Míg a ptosisban szenvedő egyéneknél a kozmézis lehet az elsődleges probléma, az előrehaladottabb esetek látótérzavarral, szemhéjfeszüléssel, a kompenzáció érdekében megváltozott fejtartással és a homlok- és fejbőrizmok megerőltetése miatti fejfájással járnak.1 Mindezek csökkenthetik a beteg életminőségét.
A következőkben ismertetjük a ptosis néhány okát, hangsúlyt fektetve a szerzett formákra, és iránymutatásokat adunk a betegek megfigyelésére és felkészítésére.
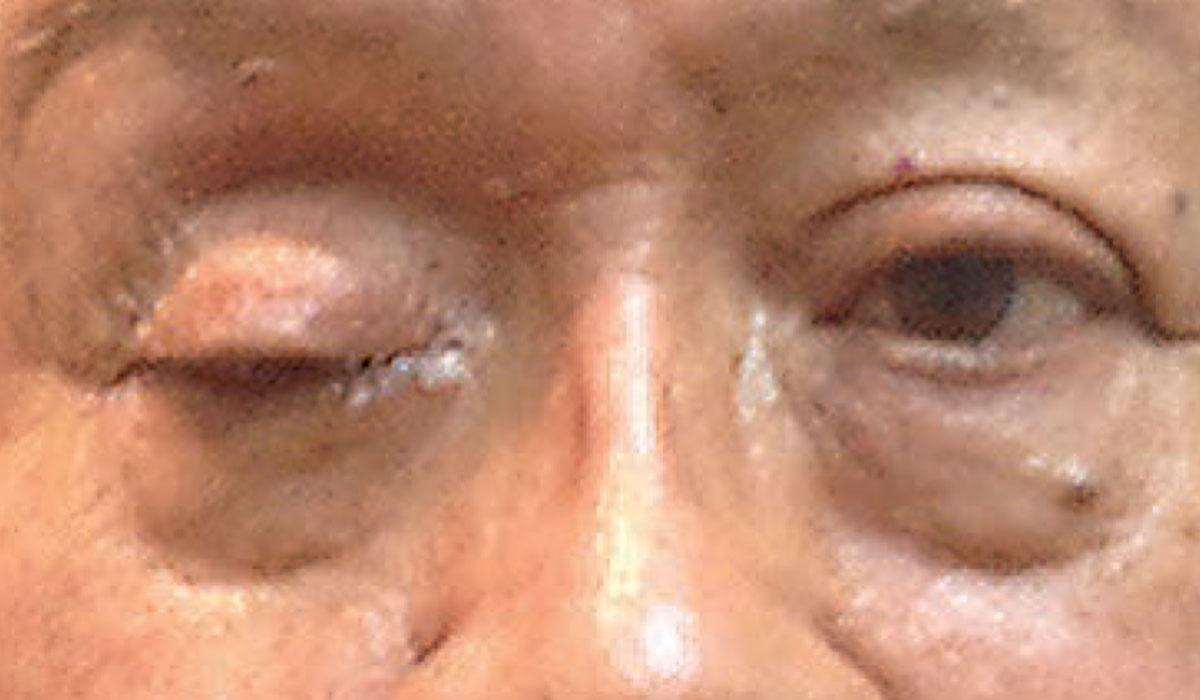
A teljes ptózis sürgős neurológiai állapot jelenlétére utalhat. Fénykép: Michael Trottini, OD. Kattintson a képre a nagyításhoz.
Anatómiai magyarázat
Mechanikai szempontból a ptosis a szemhéj felhúzásáért felelős izmok működési zavarához kapcsolódik. Ezek a felső palpebralis levator és a felső tarszális izom, más néven Müller-izom. Bármelyikük tónusának elvesztése ptózist eredményez.2 A felső palpebralis levator superior azonban a felső szemhéj fő visszahúzója, ezért működésének hiánya jelentősebb ptózist eredményez.2 A levator a nyakszirtcsont kisebb szárnyából ered, és a szemhéjba lépve legyező alakú inakkal tágul, a levator aponeurosis.2 Az aponeurosis rostjai áthatolnak az orbitalis septumon, és a felső szemhéjba nyúlva, annak teljes hosszában szétterülve, a tarsalis lemez elülső oldalára illeszkednek. A levator a III. agyideg (CN III) felső szakaszától kapja innervációját.3
A Müller-izom a levator inferior aspektusából ered, közvetlenül a fornix mögött, és a tarsalis lemez felső szélén helyezkedik el.4
Ezt az izmot szimpatikus rostok innerválják; a Müller-izom denervációja csak enyhe, 1-2 mm-es ptózist okoz.3-5
A beteg értékelése
Amikor egy egyén ptózisos panaszokkal jelentkezik, az első lépés az alapos anamnézis felvétele. Ennek magában kell foglalnia a korábbi szisztémás és szemészeti kórtörténet gondos áttekintését, az egészségi állapot és a gyógyszerhasználat esetleges változásait.
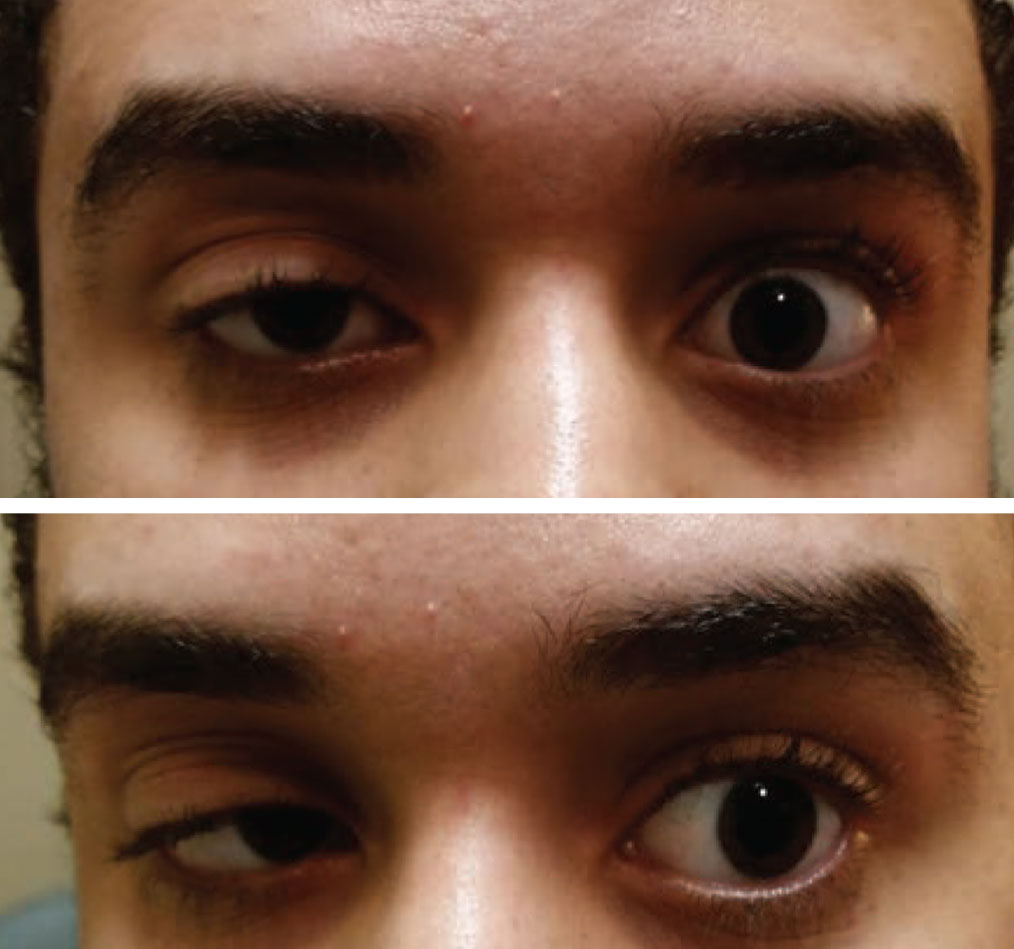
Az egyik szem szerzett ptosisát és a másik szem motilitásának korlátozását myasthenia gravisnak kell tekinteni, amíg az ellenkezőjét nem bizonyítják. Photo: Paul Ajamian, OD. Kattintson a képre a nagyításhoz.
A ptosis lehet veleszületett vagy szerzett, monokuláris vagy binokuláris és progresszív vagy nem progresszív. Ezeket a jellemzőket fel kell jegyezni a kórelőzményben, valamint a társuló neurológiai és szemészeti tünetekre, többek között homályos látásra, diplópiára, fájdalomra, perifériás térvesztésre, fejfájásra vagy generalizált izomgyengeségre való rákérdezéssel együtt. Érdeklődni kell az esetleges traumákról vagy korábbi szemműtétekről, valamint a korábbi botulinum toxin injekciókról vagy szemészeti szteroidok használatáról.6,7
A ptosis időtartamára vonatkozó kórlefolyás megismerése, valamint az, hogy a ptosis progresszív, megszűnő vagy a kezdet óta változatlan-e, fontos a napszakos változékonyságra utaló jelekkel együtt. A vizsgálatot megelőzően órákkal vagy napokkal korábban jelentkező akut kezdet komoly kóros etiológiával kapcsolatos aggodalomra ad okot.
A régi fényképek áttekintése mindig segíthet a változások megerősítésében, ha a beteg rosszul emlékszik.8
Klinikai vizsgálat
A ptosisos betegek értékelése magában foglalja az átfogó szemészeti vizsgálat számos standard összetevőjét. A látásélesség és a binokuláris látás vizsgálata segíthet a lehetséges okozó szisztémás betegség jelzésére, valamint az amblyopia vagy az elferdülés felmérésében. Ha a pácienseknél a ptosis műtéti korrekciójára kerülne sor, az amblyopia vagy a phorias jelezheti a lehetséges fúziós problémákat. A pupilla és az extraokuláris motilitás vizsgálata, valamint a szemgolyó aszimmetriájának külső megfigyelése kritikus fontosságú a későbbiekben tárgyalt egyéb kapcsolódó patológiák felméréséhez. A páciens fejpozíciójának megfigyelése és a látótér vizsgálata segíthet a ptosis hatásának és súlyosságának meghatározásában.
A szemhéjpozíció kvantitatív mérései segítenek a retraktorizmok működésének értékelésében, az anatómiai rendellenességek azonosításában, és hasznosak lehetnek a ptosis idővel történő progressziójának vagy javulásának nyomon követésében is.
Ezeket a méréseket, az úgynevezett margin reflex distance (MRD) 1, 2 és 3 méréseket elsősorban a páciens szemére irányított tolllámpával végzik, miközben a páciens elsődleges tekintetet tart. Az MRD1 esetében a felső szemhéj szélének középső része és a pupillareflex közötti távolságot milliméterben mérik mindkét szemre.9-11 A normális MRD1 4 mm és 5 mm között van.5 Az MRD1 különbség a normális és a ptotikus szem között a ptosis mértékét jelenti. Ha a ptosis elég jelentős ahhoz, hogy a pupillareflex nem látható, akkor a szemhéj milliméterben kifejezett távolságát, amelyet a szemhéjnak fel kell emelnie, amíg a pupillareflex láthatóvá válik, MRD1-ként negatív számokban rögzítik.9
Az MRD2 abban különbözik, hogy az elsődleges tekintetben, a szaruhártya fényreflexétől az alsó szemhéj központi részéig mér.12 Az MRD3 határozza meg, hogy mennyi levatort kell reszekálni azoknál a veleszületett ptosisban szenvedő betegeknél, akiknél a ptosishoz vertikális strabismus társul, és akiknél a strabismusműtét nem indikált.12
A levatorfunkciót úgy lehet mérni, hogy a felső szemhéj teljes mozgását milliméterben határozzuk meg a downgaze-től a upgaze-ig. Ez a mérés fontos a sebész számára a legmegfelelőbb korrekciós eljárás meghatározásakor. A normális levator funkció általában 15 mm-nél nagyobb, míg a 12 mm és 14 mm közötti érték jónak, az 5 mm és 11 mm közötti érték közepesnek, a 4 mm alatti érték pedig rossznak számít.5
A felső szemhéj ránc a levator aponeurosis és a felette lévő orbicularis izom találkozását jelenti. A felső szemhéj alsó szemhéjperemétől a szemhéjráncig terjedő terület általában férfiaknál körülbelül 8 mm, nőknél pedig 9-10 mm, bár ez fajonként változhat.10 A veleszületett és myogenetikus ptosisban szenvedő betegeknél a felső szemhéjránc gyakran hiányzik, vagy finom. Míg az aponeurotikus ptosisban szenvedő betegeknél a felső szemhéj ránc sokkal magasabban helyezkedik el.11
A palpebralis hasadék egyszerűen a felső és az alsó szemhéj széle közötti legszélesebb távolság az elsődleges tekintetnél, és a relatív ptosis általános összehasonlítását biztosítja. Az átlagos értékek 8 mm és 11 mm között vannak.10
A szerzett ptosis osztályozása
A vizsgálat elvégzése után a következő lépés a páciens bemutatásának osztályozása. Etiológia alapján a ptosis aponeurotikus, myogén, neurogén, mechanikus vagy traumás ptosisnak minősíthető. Lehet azonban egy úgynevezett pszeudoptózis is, amely olyan szemhéjat ír le, amely a szemhéj helyzetét közvetve befolyásoló strukturális változások miatt ptotikusnak tűnik.
Az aponeurotikus ptózis a leggyakoribb szerzett ptózis. Jellemzően idősebb egyéneknél fordul elő, de bármely életkorban jelentkezhet trauma, gyakori szemdörzsölés vagy tartós kontaktlencse-használat következtében, a kemény lencsét viselőknél nagyobb a kockázat.6 A levator funkció általában jó ezeknél a betegeknél, de a levator aponeurosis megnyúlt vagy elvékonyodott az ismétlődő stressz, valamint a gravitáció és az öregedés hatásai miatt.6 A szerzett ptosis ezen formáját mutató fiatalabb betegeknél a levator disinsertiója miatt magasabb szemhéjredő alakulhat ki.13 Ezek a betegek általában jól reagálnak a sebészeti korrekcióra.
Mechanikai ptosist okozhat bármilyen rendellenesség, amely a szemhéj szerkezetét terheli vagy megváltoztatja, beleértve a blepharochalasis, cellulitis, hordeolum, orbitális zsírprolapsus és szemhéj- vagy orbitális tumorok. Gyulladásból, műtétből, Stevens-Johnson-szindrómából vagy okuláris pemphigoidból eredő hegesedés szintén vezethet mechanikus ptosishoz.6 Mindig végezzünk orbitális képalkotó vizsgálatot olyan betegeknél, akiknél alapbetegségként tömeg vagy infiltratív elváltozás található. Az okozó tényezők kezelése a kezdeti kezelési stratégia ezeknél a betegeknél.
A traumás ptosis a szemüreg bármilyen trauma következtében kialakulhat. Az okok között szerepelhet a levator izom disszeminációja vagy a levator ín sérülése hegképződéssel. Alternatívaként a CN III sérülése is károsodhat, ami a ptózishoz vezet.6,14 Súlyos esetekben, amelyek a levator jelentős károsodását eredményezik, a betegek több műtétet is igényelhetnek, és a természetes szemhéjszimmetria helyreállításának kicsi a valószínűsége.6,14 A CN III érintettségének fokozott kockázatának kitett betegek közé tartoznak a fejsérültek, a poszttraumás sinus cavernosa trombózis, az orbitacsúcs törései és az ideg idegen testek általi kompressziója.14 A CN III károsodásban szenvedő betegek általában idővel maguktól rendeződnek, és a spontán gyógyulást három-hat hónapon keresztül kell megfigyelni, mielőtt a műtéti beavatkozást fontolóra vennék.6,14
A pszeudoptózist számos állapot eredményezheti, beleértve a blepharospasmus, a dermatochalasis csuklyával, a szemöldök ptosis, a microphthalmus, az enophthalmus és a phthisis bulbi.8 A szemhéj visszahúzódása a kontralaterális szemen, mint pajzsmirigybetegségben, szintén okozhat relatív ptotikus megjelenést a nem érintett szemhez képest.8
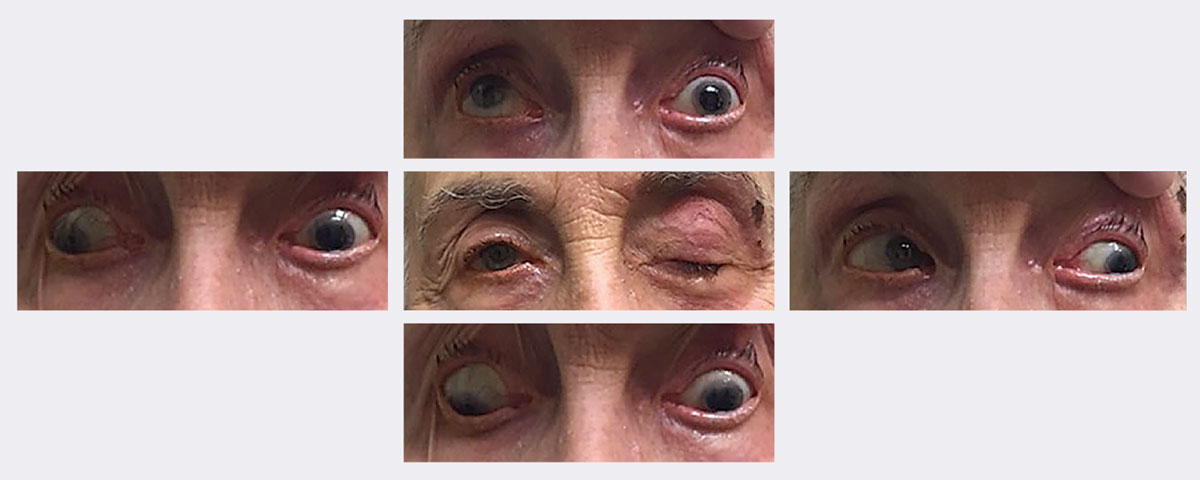
Ennek a páciensnek az első látogatáskor ptózisa volt, korlátozott felfelé és lefelé tekintéssel, valamint adductióval. Végül teljes, pupillát kímélő bal 3. idegbénulást diagnosztizáltak nála herpes zoster következtében. Antivirális készítményt használva körülbelül két hét alatt gyógyult meg. Fényképek: Michael Trottini, OD. Kattintson a képre a nagyításhoz.
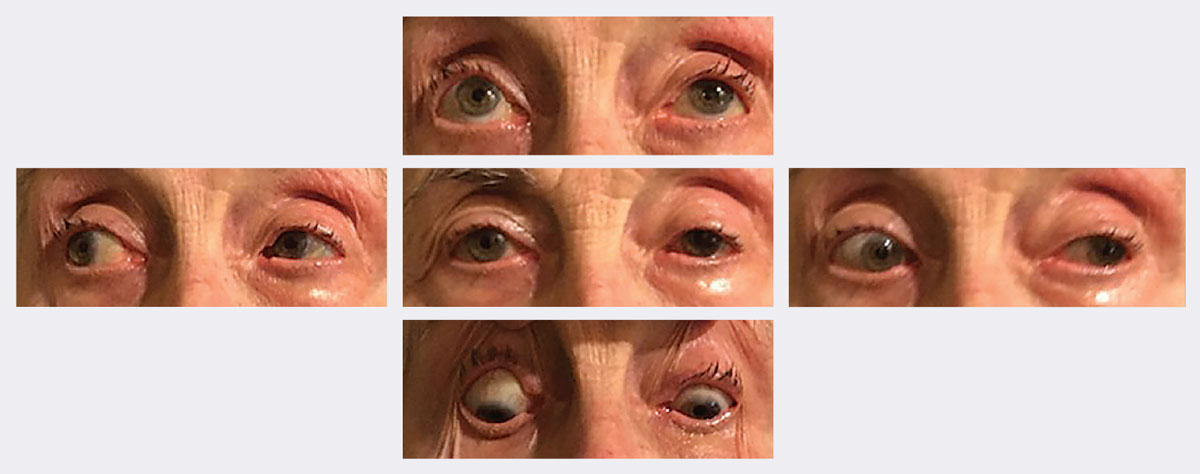
A nyomon követéskor a ptosis és a motilitás két hét alatt jelentősen javult. Photos: Michael Trottini, OD. Kattintson a képre a nagyításhoz.
Neurogén ptosis
A felső szemhéj izmainak csökkent innervációja számos lehetséges etiológiából eredhet, amelyek közül néhány életveszélyes lehet. Ezeknek az állapotoknak az azonnali azonosítása és kezelése kritikus fontosságú.
A harmadik ideg bénulása a neurogén ptosis leggyakoribb oka.1 Ez az ideg innerválja a felső, alsó és középső rectus izmokat, az inferior oblique, a levator és a pupilla sphincter izmot.15 Ha a ptosist diplopia vagy pupilla mydriasis tünetei kísérik, a harmadik ideg bénulására kell gondolni.
A harmadik idegbénulás miatt a szem “lefelé és kifelé” helyzetet vesz fel, a motilitási vizsgálat során jelentős emelési, süllyesztési és adductiós gyengeséggel.16 A harmadik idegbénulás súlyossági foka nagymértékben változhat az elváltozás okától és anatómiai elhelyezkedésétől függően.15
A harmadik idegbénulással járó ptosis lehet részleges vagy teljes. A nem teljes harmadik idegbénulással jelentkező betegeket, akiknél az extraocularis izmok csak részleges bénulása vagy csak részleges ptosis áll fenn, nagyon szorosan meg kell vizsgálni a pupillamydriázissal járó teljes bénulás progressziója szempontjából. A harmadik idegbénulással járó pupillasérülés kompressziós elváltozásra, például aneurizmára vagy daganatra utal.
A harmadik idegbénulás leggyakoribb etiológiája 50 évesnél idősebb betegeknél a mikrovaszkuláris iszkémia kardiovaszkuláris kockázati tényezők jelenlétében, ezt követi az aneurizma, a daganat, a trauma és a különböző gyulladásos és fertőző etiológiák16. A harmadik idegbénulásban és a pupillák érintettségében szenvedő betegeket sürgősen a fej idegrendszeri képalkotó vizsgálatára kell küldeni, hogy kizárják az életveszélyes aneurizmát, különösen a hátsó kommunikáló artéria aneurizmáját.15,16
A Horner-szindrómát a szem szimpatikus innervációjának megszakadása következtében kialakuló egyoldali ptosis, pupilláris miosis és arc anhidrózis jellemzi. A Horner-szindrómához társuló ptosis enyhe, jellemzően csak 1 mm és 2 mm közötti, és a felső szemhéj Müeller-izom innervációjának hiánya miatt alakul ki. A Horner-szindrómában a ptosis változó lehet, és az esetek akár 12%-ában hiányozhat is. A miózis a pupillatágító izom szimpatikus tónusának elvesztése miatt alakul ki. Az ebből eredő anisocoria sötétségben kifejezettebb, és a tágulási késés gyakran a sötétben való expozíció első öt másodpercében észlelhető.17
A Horner-szindróma a három neuronból álló oculosympatikus pálya mentén bárhol bekövetkező elváltozásból eredhet. A megerősítés történhet 0,5%-os apraclonidinnel vagy ritkábban kokainnal végzett farmakológiai vizsgálattal.17,18 A pozitív apraclonidin-teszt a miotikus pupilla tágulását eredményezi az írisztágító izom túlérzékenysége miatt, valamint a szemhéj helyzetének normalizálódását.1,17
A hidroxi-amfetamin használható annak megállapítására, hogy az elváltozás pre- vagy posztganglionáris-e; ezt azonban a modern gyakorlatban ritkán alkalmazzák, mivel neuroimaginget általában ettől függetlenül rendelnek.17,18
Myasthenia Gravis tesztelés
Két, a vizsgálóban könnyen elvégezhető teszt a myasthenia gravis felmérésére a nyugalmi és a jeges teszt. A nyugalmi teszthez a ptosisban szenvedő betegeknek azt kell mondani, hogy két percig óvatosan tartsák csukva a szemüket. A myasthenia gravisban szenvedő betegek körülbelül 50%-ánál a nyugalmi teszt során a ptosis legalább 2 mm-es javulást mutat.1 A kutatók úgy vélik, hogy ez azért történik, mert a szinapszisban felhalmozódik az ACh mennyisége, ami javítja az izomreakciót.
A jégtesztet úgy végzik, hogy két percre jeget helyeznek a ptotikus szemhéjra, majd újraértékelik a ptózist. A nyugalmi teszthez hasonlóan a 2 mm-es vagy annál nagyobb javulás pozitív teszteredménynek számít.1,2 Az egyéb okokra visszavezethető ptosis nem javul sem a nyugalmi, sem a jeges teszttel.1
A myasthenia gyanúja esetén AChR antitestek laboratóriumi vizsgálatát is el kell végezni. Ne feledjük, hogy a tisztán szemészeti myasthenia gravisban szenvedő betegek 30-65%-a szeronegatív.3,4 A vizsgálatok azt mutatják, hogy az AChR-antitestek szintje nem korrelál a betegség súlyosságával, és nem segít annak előrejelzésében, hogy ki fog generalizált betegséget kialakítani.3,5
A Tensilon-tesztet sokáig a myasthenia gravis elsődleges diagnosztikai vizsgálatának tekintették, bár ma már ritkábban alkalmazzák, mint korábban, a szívpanaszok, a szinkópa és a kolinerg krízis kockázata miatt. A hamis negatív és hamis pozitív eredmények nagy gyakorisággal fordulnak elő.1
1. Kubis K, Danesh-Meyer H, Savino P, Sergott R. A jégteszt versus a nyugalmi teszt myasthenia gravisban. Ophthalmol. 2000;107(11):1995-8.
2. Ellis F, Hoyt C, Ellis F, et al. Extraocular muscle responses to orbital cooling (ice test) for ocular myasthenia gravis diagnosis. J AAPOS Off Publ Am Assoc Pediatr Ophthalmol Strabismus. 2000;4(5):271-81.
3. Monsul N, Patwa H, Knorr A, et al. The effect of prednisone on the progression from ocular to generalized myasthenia gravis. J Neurol Sci. 2004;217(2):131-3.
4. Porter N, Salter B. Szemészeti myasthenia gravis. Curr Treat Options Neurol. 2005;7(1):79-88.
5. Kupersmith MJ. Szemészeti myasthenia gravis: kezelési sikerek és kudarcok hosszú távú követéssel rendelkező betegeknél. J Neurol. 2009;256(8):1314-20.
Felnőttek esetében nincs szükség képalkotásra, kivéve, ha a Horner-szindróma akut fájdalommal jár. A legújabb tanulmányok amellett érvelnek, hogy az újonnan kezdődő izolált Horner-szindrómás, lokalizáló jelek vagy tünetek nélküli betegeknél a képalkotásnak a teljes oculosympatikus pályára kell összpontosítania MRI és angiográfia segítségével, mivel a lehetséges etiológiák oly számosak. Az okozó elváltozás jellemzően az esetek 20%-ában azonosítható, a leggyakoribb az arteria carotis dissectio, amely spontán vagy trauma következtében is kialakulhat.
Más súlyos etiológiák, amelyeket ki kell zárni, a rosszindulatú daganat, az agytörzs érrendszeri elváltozásai és a sinus cavernosus trombózisa.1,17,18 A régóta fennálló Horner-szindróma esetében, amelyet jellemzően két éve vagy annál hosszabb ideje tartanak fenn, a képalkotás nem feltétlenül indokolt, hacsak nem jelentkeznek új tünetek.17
A myasthenia gravis egy ritka rendellenesség, amelyet a nikotinos acetilkolin-receptor (AChR) ellen irányuló antitest-közvetített immuntámadás jellemez.19 A betegek akár 65%-ánál a myasthenia gravis kezdeti jelei és tünetei közé tartozik a ptosis, az extraocularis izomgyengeség, az orbicularis oculi gyengesége vagy a szem félrenézése.20 A tünetek egy- vagy kétoldaliak lehetnek, általában visszatérőek és változóak, a fáradtsággal fokozatosan romlanak. Jellemzően a betegek több mint 90%-ánál a betegség lefolyása során valamilyen mértékben jelentkeznek ezek a tünetek.21,22 A tisztán szemészeti myasthenia gravis körülbelül 50%-ban fordul elő.21 Körülbelül a betegek fele két éven belül generalizált betegséggé alakul át.23-25
A megerősített vagy akár csak gyanús myastheniás betegeknél CT-képalkotást is kell végezni a thymus hyperplasia vagy thymoma kimutatására.21 A thymoma a myastheniás betegek körülbelül 10-15%-ánál fordul elő és sebészi reszekciót igényel.26
Myogenetikus ptosis
Ez a leggyakoribb veleszületett ptosis lehet szerzett vagy veleszületett, és a levator izom dysgenesiséből ered, a vázizomrostok helyén fibroadipóz szövet található.6 A szerzett myogenetikus ptosis a tipikusan kétoldali progresszív ptosis ritka formáját írja le, amelyet szisztémás izomzavarok okoznak.6,27,28 Ide tartozhat az izomdisztrófia, a myasthenia gravis (korábban tárgyalt), az oculopharyngealis dystrophia és a krónikus progresszív külső szemtengelyferdülés (CPEO).6 Ritkábban szteroid-indukált és HAART-asszociált myogén ptosisról számoltak be.27,28
A myotonikus dystrophia a felnőttkori izomdystrophia leggyakoribb formája. A szemészeti leletek közé tartozik a szimmetrikus ptosis, a blepharospasmus, a szemgörcs és a karácsonyfa-katarakták. A kezdeti tünet gyakran a myotonia (a vázizomzat késleltetett elernyedése az összehúzódás után); így az érintetteknél a szemtünetek megjelenése előtt is diagnosztizálható. Az érintett betegeknél korai frontális alopecia, a halánték- és a rágóizmok elsorvadása és a végtagok distalis gyengesége is jelentkezhet, amit hideg, izgalom vagy fáradtság súlyosbít.29,30 A légzőszervi megbetegedések és a szívmyopathia a leggyakoribb halálokok.30
A myogenetikus ptosis korrigálható szemhéjmankóval vagy műtéttel; azonban óvatosan kell eljárni, amikor bármelyiket javasoljuk, mivel ezeknél a betegeknél a rossz Bell-jelenség és a nem teljes pislogás miatt nagyobb a kockázata a posztoperatív szemszárazságnak és az expozíciós keratopátiának.31,32
Ha egy beteg ptózissal jelentkezik, az alapos anamnézis és klinikai vizsgálat döntő fontosságú annak meghatározásában, hogy mikor van szükség további kivizsgálásra vagy beutalásra, mivel a ptózis számos potenciálisan halálos kimenetelű betegség kezdeti tünete lehet.
Általános klinikai gyöngyszemként minden olyan esetben, amikor a klinikai vizsgálat során ptosis, pupillaanomália, extraocularis motilitási zavar, globus aszimmetria vagy dystopia észlelhető, mindegyik alapos értékelése indokolt, mivel ezek egyidejű betegségre utalhatnak.8,33 Az etiológiától függően a ptosis egyes esetei spontán megszűnnek, mások a szisztémás betegség kezelését igénylik, és néhány esetben műtétre van szükség. Mint minden beavatkozásnál, a műtét utáni szövődmények is előfordulhatnak, beleértve, de nem kizárólagosan az alul- és túlkorrekciót, ami lagophthalmushoz és szemszárazsághoz vezet, a szemhéjredő rendellenességeket és a szemhéjperem torzulását.
A szemésznek tisztában kell lennie a lehetséges etiológiákkal, és képesnek kell lennie felismerni, hogy a ptosis megjelenése mikor jelent sürgős helyzetet, amely azonnali diagnosztikai vizsgálatot, kezelést és beutalást igényel.
Reinhard és Spampinato doktorok a Cincinnati Veteran’s Administration Medical Center optometristái és az Ohio State University College of Optometry adjunktusai.
1. Díaz-Manera J, Luna S, Roig C. Ocularis ptosis: differenciáldiagnózis és kezelés. Curr Opin Neurol. 2018;31(5):618-627.
2. Oyster CW. Az emberi szem: szerkezet és működés. Sunderland, MA: Sinauer Associates; 2006.
3. Remington, L.A. Clinical Anatomy of the Visual System (Second Edition). Butterworth-Heinemann; 2005.
4. Ezra DG, Beaconsfield M, Collin R. Surgical anatomy of the upper eyelid: Old controversies, new concepts. Expert Rev Ophthalmol. 2009;4(1):47-57.
5. Pauly M, Sruthi R. (2019). Ptosis: Értékelés és kezelés. Kerala J Ophthalmol. 2019;31(1);11-16.
6. Finsterer J. Ptosis: okok, bemutatás és kezelés. Aesthetic Plast Surg. 2003;27(3):193-204.
7. Iliff JW, Pacheco EM. Duane’s Clinical Ophthalmology. (Tasman W, Jaeger E, szerk.). Lippincott Williams and Wilkins; 2001.
8. Latting MW, Huggins AB, Marx DP, Giacometti JN. A blepharoptosis klinikai értékelése: az életkorral összefüggő ptosis megkülönböztetése a maszkszerű állapotoktól. Semin Plast Surg. 2017;31(1):5-16.
9. Putterman AM. Margin reflex distance (MRD) 1, 2, and 3: Ophthal Plast Reconstr Surg. 2012;28(4):308-11.
10. Yadegari S. A blepharoptosisban szenvedő beteg megközelítése. Neurol Sci. 2016;37(10):1589-96.
11. Lim J, Hou J, Singa R, et al. A blepharoptosis altípusainak relatív előfordulása egy tercier ellátóközpont szemészeti rendelőjében. Orbit. 2013;32(4):231-4.
12. Burkat C, Oh D, Yen M. Margin to reflex distance 1,2,3. Eyewiki. eyewiki.aao.org/Margin_to_reflex_distance_1,2,3. September 16, 2019. Hozzáférés 2020. március 13.
13. Savar A, Blaydon S, Nakra T, Shore J. Ptosis sebészet: In: Tasman W, Jaeger E eds. Duane’s Ophthalmology. Pennsylvania: Lippincott Williams & Wilkins; 2013.
14. Jacobs SM, Tyring AJ, Amadi AJ. Traumás ptosis: az etiológia, a kezelés és a prognózis értékelése. J Ophthalmic Vis Res. 2018;13(4):447-52.
15. Bhatti MT, Eisenschenk S, Roper SN, Guy JR. Superior divizionális harmadik koponyaideg paresis: klinikai és anatómiai megfigyelések 2 egyedi esetről. Arch Neurol. 2006;63(5):771-6.
16. Kung N, Stavern GPV. Izolált szemmozgató idegbénulások. Semin Neurol. 2015;35(05):539-48.
17. Martin TJ. Horner-szindróma: klinikai áttekintés. ACS Chem Neurosci. 2018;9(2):177-186.
18. Beebe J, Kardon R, Thurtell M. A képalkotó diagnosztika hozadéka izolált Horner-szindrómás betegeknél. Neurol Clin. 2017;35(1):145-51.
19. McGrogan A, Sneddon S, Vries CS de. A myasthenia gravis előfordulása: szisztematikus irodalmi áttekintés. Neuroepidemiológia. 2010;34(3):171-83.
20. Kupersmith MJ. Szemészeti myasthenia gravis: kezelési sikerek és kudarcok hosszú távú követéssel rendelkező betegeknél. J Neurol. 2009;256(8):1314-20.
21. Gilbert ME, Savino PJ. Szemészeti myasthenia gravis. Int Ophthalmol Clin. 2007;47(4):93-103.
22. Antonio-Santos AA, Eggenberger ER. Az okuláris myasthenia gravis gyógyszeres kezelési lehetőségei. Curr Opin Ophthalmol. 2008;19(6):468-478.
23. Porter NC, Salter BC. Ocular myasthenia gravis. Curr Treat Options Neurol. 2005;7(1):79-88.
24. Gilbert M, De Sousa E, Savino P. Ocularis myasthenia gravis kezelése: a prednizonterápia és a thymectomia ellen. Arch Neurol. Dec 2007 (64):1790-2.
25. Kumar V, Kaminski HJ. A myasthenia gravis kezelése. Curr Neurol Neurosci Rep. 2011;11(1):89-96.
26. Silvestri N, Wolfe G. Myasthenia Gravis. Semin Neurol. 2012;32(03):215-226.
27. Song A, Carter K, Nerad J, et al. Steroidok okozta ptosis: esettanulmányok és szövettani elemzés. Eye. 2008;22(4):491-5.
28. Silkis R, Lee H, Gills Ray V. Highly Active Antiretroviral Therapy-Associated Ptosis in Patients With Human Immunodeficiency Virus. Arch Ophthalmol. 2009;127(3):345-6.
27. Kubis KC, Danesh-Meyer HV, Savino PJ, Sergott RC. A jégteszt versus a nyugalmi teszt myasthenia gravisban. Ophthalmol. 2000;107(11):1995-8.
28. Ellis F, Hoyt C, Ellis F, et al. Extraocular muscle responses to orbital cooling (ice test) for ocular myasthenia gravis diagnosis. J AAPOS. 2000;4(5):271-81.
29. Nguyen C, Campbell C. 1-es típusú myotonikus dystrophia. CMAJ Can Med Assoc J. 2016;188(14):1033.
30. Thornton CA. Myotonikus dystrophia. Neurol Clin. 2014;32(3):705-19.
31. de Castro FAA, Cruz AAV, Sobreira CF da R. Brow Motility in Mitochondrial Myopathy: Ophthal Plast Reconstr Surg. 2010;26(6):416-9.
32. Daut P, Steinemann T, Westfall C. Chronic exposure keratopathia complicating surgical correction of ptosis in patients with chronic progressive external ophthalmoplegia. Am J Ophthalmol. 2000;130(4):519-21.
33. Murchison AP, Bilyk JR, Savino PJ. Ptosis neurológiai betegségben. In: Black E, Nesi F, Calvano C, et al, eds. Smith and Nesi’s Ophthalmic Plastic and Reconstructive Surgery. New York, NY: Springer; 2012:361-92.