
Niemal jedna trzecia z 7,25 mld ludzi na ziemi, w tym szacunkowo 60 mln ludzi w Stanach Zjednoczonych, jest przewlekle zakażona pierwotniakiem Toxoplasma gondii. Sprawny układ odpornościowy jest w stanie utrzymać pasożyta w ryzach, więc tylko mniejszość zarażonych ma znaczące objawy. Ale kiedy niczego nie podejrzewająca kobieta zaraża się podczas ciąży i przekazuje pasożyta swojemu nienarodzonemu dziecku, konsekwencje mogą być głębokie.
Obejmują one wyniszczające uszkodzenia mózgu, układu nerwowego i oczu. Teraz pojawia się coraz więcej dowodów na to, że niektórzy ludzie, a może nawet wiele osób, mają subtelniejsze objawy wywołane przez zakażenie. Być może odpowiedź immunologiczna, utrzymując pasożyty w ryzach, powoduje uboczne uszkodzenia w innych miejscach. A może pasożyty, które produkują neuroprzekaźnik dopaminę i współdziałają z komórkami, które infekuje, modyfikuje zachowanie swojego gospodarza.Zapytaliśmy wiodący autorytet w sprawie Toxoplasma gondii i toksoplazmozy, Rima McLeod, MD, profesor okulistyki & nauki o wzroku i pediatrii oraz dyrektor medyczny centrum toksoplazmozy na Uniwersytecie w Chicago, wielkie pytanie: Jak myślimy, co się dzieje, gdy miliardy ludzi przechodzą przez życie z pasożytniczą infekcją mózgu?
Na początek, czym jest Toxoplasma gondii?
Rima McLeod: Toxoplasma gondii jest mikroskopijnym pasożytem spokrewnionym z pasożytem, który powoduje malarię. Ma kilka etapów cyklu życiowego.
Jest to pasożyt o równych szansach. Zaraża osoby na całym świecie, bez względu na miejsce, pochodzenie etniczne czy status społeczno-ekonomiczny, chociaż genetyka żywiciela odgrywa ważną rolę w manifestacji zakażenia.
A co z toksoplazmozą?
Toksoplazmoza odnosi się do chorób wywoływanych przez tego pasożyta. Powinienem powiedzieć pasożytów. Dowiadujemy się, że genetycznie różne pasożyty różnią się chorobami, które wywołują, często różniącymi się w zależności od położenia geograficznego. Na przykład, różne typy genetyczne pasożytów są obecne w różnych regionach klimatycznych USA, powodując różne nasilenie choroby.
Pasożyt może powodować choroby w ostrej, aktywnej formie, gdy nabyte przez starsze dzieci i dorosłych. Czasami uszkadza oko i sporadycznie serce lub mózg lub powoduje powiększenie węzłów chłonnych. Jest to najczęstsza zakaźna przyczyna zniszczenia tylnej części gałki ocznej. Następnie przechodzi w stan uśpienia, ale może się odrodzić w aktywnej, niszczącej formie, gdy układ odpornościowy nie jest w normie, np. u osób z nowotworami złośliwymi lub AIDS lub podczas leczenia, które tłumi układ odpornościowy. W takim przypadku pasożyt może uszkodzić mózg lub inne narządy.
Gdy kobieta nabywa zakażenie po raz pierwszy, gdy jest w ciąży i przenosi pasożyta na swój płód, powoduje to wrodzone zakażenie pasożytnicze. Może to być straszna choroba, gdy nie jest leczona lub złapana zbyt późno. W takiej sytuacji może spowodować utratę wzroku, ciężkie zapalenie mózgu i trwałe uszkodzenia neurologiczne.

Nawet gdy nie ma poważnych objawów przy urodzeniu, może przejść z fazy uśpionej do aktywnej i spowodować nowe uszkodzenia oka i mózgu. Dlatego tak ważne są badania przesiewowe w kierunku zakażenia u kobiet w ciąży.
Jak ludzie zarażają się tą chorobą?
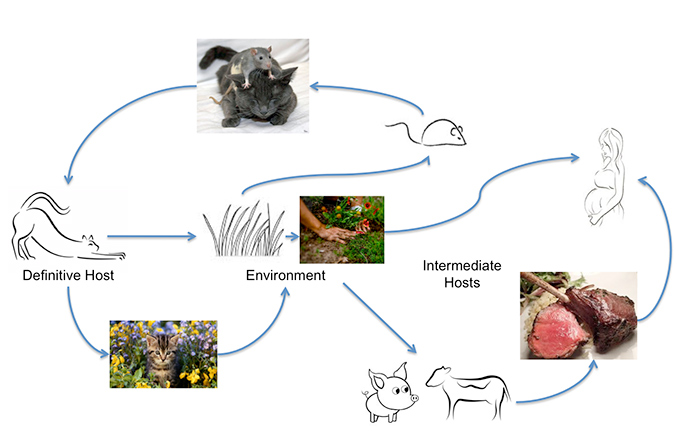
Toksoplazma gondii może zarazić większość zwierząt ciepłokrwistych, w tym ludzi, ale głównym gospodarzem, u którego dochodzi do wymiany genetycznej są koty. Ludzie mogą zarazić się poprzez spożycie niedogotowanego mięsa lub oocyst wydalanych przez koty, znajdujących się na przykład na nieumytych warzywach lub w skażonej wodzie. Nierozpoznany kontakt z oocystami może się łatwo zdarzyć, ponieważ ostro zarażony kot może wydalić do 500 milionów oocyst Toxoplasma w ciągu dwóch tygodni. Nawet jedna oocysta jest zakaźna. Przetrwają one w ciepłej, wilgotnej glebie i wodzie przez rok. Badanie przeprowadzone przez Johns Hopkins University wykazało, że roczne obciążenie oocystami mierzone w badaniach społeczności wynosi od trzech do 434 oocyst na stopę kwadratową. Te liczby idą w górę, dodają, „w obszarach, gdzie koty selektywnie defekacji”. To dlatego zakażenie jest tak powszechne.
OK. To jest niepokojące. Co się stanie, gdy ktoś połknie kilka oocyst?
T. gondii jest pasożytem obligatoryjnie wewnątrzkomórkowym. Oznacza to, że aby przeżyć, musi zainfekować komórki gospodarza. Komórki, w których najchętniej przebywa, gdy jest w stadium uśpienia, znajdują się w mózgu i siatkówce, w tylnej części oka. Zakaża, a następnie ukrywa się i powoli replikuje w tych komórkach. To jest przewlekła, trwająca całe życie infekcja.
Co się dzieje z ludźmi, którzy mają normalną odporność i nie byli narażeni przed urodzeniem, którzy później zarażają się pasożytami?
Wielu lekarzy uważa takie utajone lub bezobjawowe przypadki za klinicznie nieistotne. W mojej grupie badawczej i laboratorium, skupiliśmy się na biologii aktywnych infekcji, szczególnie u dzieci, i jak najlepiej im zapobiegać i leczyć. Jednak od ponad dekady prowadzone są liczne badania nad subtelnymi, lub nie tak subtelnymi, zmianami w zachowaniu zwierząt związanymi z utajonym zakażeniem T. gondii. Na przykład myszy i szczury z infekcją tracą awersję do zapachu kotów, a zwłaszcza do kociego moczu. Ten tzw. śmiertelny koci pociąg jest niebezpieczny dla wszystkich gryzoni, które w wyniku zakażenia stały się nieustraszone; ułatwia on kotom ich łapanie i zjadanie. Ale jest to korzystne dla kotów, które zdobywają łatwy posiłek i pomaga pasożytom, które zyskują nowy rezerwuar.Stwierdziliśmy, że przewlekle zarażone myszy mają dodatkowe zmiany behawioralne, takie jak zamarzanie w otwartym terenie, gorzej się pielęgnują, tracą równowagę i zmniejszają siłę chwytu. Zachowania te są typowe dla niezdrowego starzenia się. Mózgi chronicznie zarażonych myszy są mniejsze niż mózgi normalnych osobników. Znajdujemy pasożyty w cystach wewnątrz neuronów, które utworzyły synapsy. Widzimy również proces zapalny, szczególnie w obrębie i obok części mózgu związanej z pamięcią.

Czy istnieje ludzki odpowiednik takich zmian w zachowaniu?
Kiedyś miałem wątpliwości, ale nie jestem już tak pewny, że ta behawioralna zmiana dotyczy tylko gryzoni. Ostatnie badanie ze Stanforda wykazało zmiany w cząsteczkach układu odpornościowego we krwi chronicznie i ostro zakażonych ciężarnych kobiet, które nie były obecne w niezakażonych, dopasowanych kontrolach. Grupa z Uniwersytetu Johnsa Hopkinsa odkryła subtelne, ale specyficzne deficyty pamięci u młodych profesjonalistów, którzy mieli przeciwciała przeciwko pasożytowi, w porównaniu z dopasowanymi kontrolami.Kilka zespołów badawczych szukało wpływu na osobowość lub zachowanie u ludzi. Grupy te stwierdziły, że pacjenci ze schizofrenią lub zaburzeniami obsesyjno-kompulsywnymi są statystycznie bardziej narażeni na infekcję T. gondii. Zakażeni mężczyźni mają wolniejszy czas reakcji i ponad dwa razy więcej wypadków drogowych. Istnieją również związki pomiędzy posiadaniem przeciwciał przeciwko pasożytowi a chorobą dwubiegunową, zachowaniami samobójczymi, a nawet optymistycznym usposobieniem, prawdopodobnie związanym z wpływem pasożyta na dopaminę. W analizie z 2012 roku przeprowadzonej we Francji, gdzie szacuje się, że 43 procent ludzi jest nosicielami T. gondii, stwierdzono, że mężczyźni z utajonym zakażeniem mają tendencję do bycia „bardziej dogmatycznymi, mniej pewnymi siebie, bardziej zazdrosnymi, mniej impulsywnymi i bardziej uporządkowanymi niż niezakażeni mężczyźni”. Zakażone kobiety wydawały się cieplejsze, bardziej sumienne, bardziej wytrwałe, bardziej niepewne i bardziej świętoszkowate.”
Jak się mierzy świętoszkowatość?
Nie wiem co z tego zrobić, ani z wielu badań asocjacyjnych, ponieważ trudno jest wiedzieć co było pierwsze: infekcja czy cecha. Jest jeden naukowiec, który uważa, że jest przyziemnym przykładem pierwszej osoby. Czeski badacz Jaroslav Flegr, profesor Uniwersytetu Karola w Pradze, mówi i pisze o zmianach, jakie zauważył w swoim zachowaniu po zarażeniu się T. gondii. Twierdzi on, że utajone infekcje Toxoplasma sprawiły, że mężczyźni stali się bardziej skłonni do wycofania się, stali się wrodzy, aspołeczni lub wręcz „kurduplowaci”. Zarażone kobiety, z drugiej strony, szukają ukojenia poprzez tworzenie więzi społecznych i pielęgnację. Są skłonne do czułości i przyjaźni. Flegr był znany z tego, że porównywał je do „seksownych kociąt”. Nie pytajcie mnie, jak to się ma do świętości. Tego typu informacje są w literaturze, ale nie są ostatecznie udowodnione jako przyczyna i skutek w chwili obecnej.
Ponownie, zrzędliwe zachowanie może być trudne do zmierzenia, tak?
Dokładnie, więc nasze laboratorium woli skupić się na zrozumieniu jak T. gondii wyrządzają szkody, geny, które inicjują ten proces, jak również te, które chronią przed infekcją Toxoplasma. Chcemy opracować leki, które będą w stanie wyleczyć chorobę i stworzyć szczepionkę, która będzie jej zapobiegać. Naszym długoterminowym celem jest zrozumienie tej choroby w celu poprawy leczenia i wyników.W procesie naszych badań genetycznych, jednak natknęliśmy się na wiele połączeń między szlakami genetycznymi, które pomagają kontrolować infekcję T. gondii i tych implikowanych w chorobach neurobehawioralnych i neurodegeneracji. Coraz bardziej podejrzewam, że ten pasożyt – poprzez odpowiedź układu odpornościowego na niego i bezpośrednie interakcje pasożytów z macierzystymi i zróżnicowanymi komórkami neuronów gospodarza – wpływa na te same szlaki, które są związane z zaburzeniami neurologicznymi, w tym z chorobą Alzheimera i prawdopodobnie autyzmem. I wskazuje na wskazówki dotyczące tego, w jaki sposób pasożyt może przyczynić się do tych chorób u niektórych genetycznie podatnych osób narażonych na nie.
Jak nawiązaliście połączenie?
Przyjrzeliśmy się bliżej genom zaangażowanym w ochronę gospodarza przed tym pasożytem. Badanie z 2006 roku z Francji zidentyfikowało mały region na chromosomie 10 szczura, obecnie nazywany Toxo1. Region ten zawiera około 30 genów. Odkryto, że niektóre z tych genów odgrywają główną rolę w zapobieganiu proliferacji i rozprzestrzeniania się pasożyta w komórkach szczura. Co ciekawe, geny chroniące przed Toxo pochodzą od szczurów Lewis, standardowych, potulnych, eksperymentalnych zwierząt hodowanych od pokoleń w laboratorium. Geny, które nie zapobiegają Toxo, są powszechne u brązowych szczurów norweskich, twardzieli, których wielu ludzi nazywa „szczurami kanałowymi”. W tym czasie nasi koledzy z Francji, z uniwersytetów w Grenoble i Tuluzie, mieli trudności z ustaleniem, które geny w tym regionie mogą być kluczowe. Ich praca na szczurach skłoniła nas do szukania podobieństw w tym regionie genowym u ludzi. To zapoczątkowało nasze badania mające na celu wyśledzenie podobnego zestawu genów, z kilkoma znaczącymi różnicami, na ludzkim chromosomie 17. Dekady pracy z pacjentami dały nam ogromną przewagę. Śledzimy około 250 rodzin – każda z nich obejmuje matkę, ojca i dziecko zarażone Toxoplasma in utero. W około 20 z tych rodzin mamy zestawy bliźniąt, które były narażone razem. W niektórych przypadkach mamy identyczne bliźnięta, oboje bardzo chorzy, z takimi samymi objawami zakażenia. W innych przypadkach objawy są minimalne. W przypadkach nieidentycznych bliźniąt, czasami jedno z nich jest głęboko dotknięte chorobą, a drugie wydaje się normalne. Wiemy więc, że dziedziczenie wariantów genów ochronnych lub podatności od matki i ojca może mieć znaczenie. Obecnie uważnie przyglądamy się każdemu z tych i dodatkowych genów.
Co robią te geny i czego się dowiedzieliście? Właśnie opublikowaliśmy pracę na temat ALOX12 w czasopiśmie Infection and Immunity. Jesteśmy na wczesnym etapie procesu badania wszystkich genów, ale dotychczasowe wyniki są fascynujące. Zastosowaliśmy podejście oparte na genach kandydujących. Pierwsze dwa badane przez nas geny, po jednym z obu końców regionu Toxo1, miały warianty, które korelowały na wysokim poziomie z podatnością lub opornością. Wcześniej znaleźliśmy to w genie znajdującym się w dolnej części regionu, znanym wówczas jako caterpillar. W obecnej pracy znaleźliśmy to w genie znajdującym się na górze regionu, zwanym ALOX12. Jest to gen śmierci komórkowej.
Technicznie jest to lipooksygenaza, która dodaje toksyczny, niestabilny tlen do 12. węgla kwasu arachidonowego – tworząc biologicznie szkodliwą cząsteczkę. Inni znaleźli dowody na to, że ALOX12 wpływa na wyniki w cukrzycy, chorobach neurodegeneracyjnych i schizofrenii, ale nic nie było wiadomo o jego roli w chorobach zakaźnych.Kiedy przetestowaliśmy odmiany tego genu od różnych rodziców i dzieci, odkryliśmy, że niektóre allele – szczególne odmiany czterech części genu – były znacząco różne, i że te różnice były związane z podatnością. Kiedy zredukowaliśmy ALOX12, aktywność zapalna i śmierć komórek, które chronią przed toksoplazmozą, zmniejszyła się. Stało się prawdopodobne, że pewne warianty tego genu były bardziej skuteczne niż inne w wyzwalaniu stanu zapalnego i zabijaniu zainfekowanych i pobliskich komórek oraz pasożytów. Z produktem enzymatycznym tego genu był silniejszy efekt w utrzymywaniu infekcji zawartej w ludzkich komórkach. Bez produktu tego genu te same komórki nie były w stanie powstrzymać infekcji. Kiedy testowaliśmy te komórki z nieaktywnym genem ALOX12, pasożyty rozmnażały się błyskawicznie. Inny gen na drugim końcu regionu, znany jako caterpillar lub NALP1, miał podobny efekt. Opublikowaliśmy to w 2011 roku.
Czy istnieje minus tych agresywnych genów przeciwpasożytniczych?
Te czynniki śmierci komórkowej znalezione w tym krytycznym skupisku genów zwanym Toxo1 są ważne w ograniczaniu tej infekcji. Ale teraz podejrzewamy, że wysoka aktywność tych genów w późniejszym okresie życia może mieć szkodliwy efekt, zabijając nie tylko komórki gospodarza pasożytów, ale także niewinnych przechodniów. Jest to przypuszczenie, ale może pomóc wyjaśnić, dlaczego polimorfizm genu, który wydaje się odgrywać rolę w początkach chorób związanych ze starzeniem się, może nadal być preferowany przez ewolucję za jego zdolność do zapobiegania lub kontrolowania powszechnej infekcji we wczesnym okresie życia, zwłaszcza do wieku rozrodczego.
Dlaczego te geny skupiłyby swoje efekty na zachowaniu lub chorobie neurologicznej?
Toksoplazma infekuje komórki nerwowe. Niektóre wersje ALOX12 i NALP1 mogą pomóc zainfekowanej osobie w uzyskaniu silnej, wczesnej, ochronnej odpowiedzi immunologicznej, zabijającej pasożyty, zainfekowane komórki, jak również pobliskie komórki. Ale wiemy również, że ALOX12 jest związany z chorobami związanymi ze starzeniem się i utratą pamięci. Kiedy wykorzystaliśmy nasze odkrycia dotyczące ALOX12 z programami biologii systemów, używanymi do mapowania ścieżek, zdaliśmy sobie sprawę, że wiele z tych ścieżek jest również w grze w różnych chorobach neurodegeneracyjnych, takich jak choroba Alzheimera, a nawet schizofrenia. Niektóre z nich mogą przyczyniać się do rozwoju miażdżycy lub cukrzycy. Kiedy ta potężna odpowiedź immunologiczna pozostaje w pracy, może mieć efekty, które mogą być szkodliwe.Bardziej skuteczne leki lub szczepionka mogłyby chronić przed niszczącymi chorobami, które powoduje ten pasożyt. Ta ostatnia praca podnosi możliwość, że lepsze leczenie, poprzez szybkie kontrolowanie lub eliminowanie infekcji, może również zmniejszyć choroby związane z wiekiem, które spekulujemy, mogą wiązać się z toksoplazmą dla niektórych ludzi.
To jest duży projekt. Wydaje się, że masz wielu partnerów w tym wysiłku, tak?
To była wspaniała współpraca z kolegami we Francji, Anglii i Kanadzie oraz zespołem na Uniwersytecie w Kansas, wraz z pracą niezwykłej grupy młodych naukowców w moim własnym laboratorium.

To jest zachęcające. Z kim pracujesz, aby posunąć to odkrycie do przodu?
Pracujemy w naszych własnych programach badawczych i grupie laboratoryjnej oraz z kolegami w New Haven, Instytucie J Craiga Ventnera i Instytucie Biologii Systemów w Seattle oraz z wieloma innymi kolegami. Jesteśmy bardzo podekscytowani spostrzeżeniami i możliwościami rozwoju profilaktyki i leczenia, które zapewnia ta praca.
.