
Nahezu ein Drittel der 7,25 Milliarden Menschen auf der Erde, darunter schätzungsweise 60 Millionen Menschen in den Vereinigten Staaten, sind chronisch mit dem Protozoon Toxoplasma gondii infiziert. Ein funktionierendes Immunsystem kann den Parasiten in Schach halten, so dass nur eine Minderheit der Infizierten nennenswerte Symptome aufweist. Wenn sich jedoch eine ahnungslose Frau während der Schwangerschaft infiziert und den Parasiten auf ihr ungeborenes Kind überträgt, kann dies schwerwiegende Folgen haben: verheerende Schäden an Gehirn, Nervensystem und Augen. Nun mehren sich die Hinweise darauf, dass manche Menschen, vielleicht sogar viele, subtilere Symptome haben, die durch die Infektion ausgelöst werden. Vielleicht hält die Immunreaktion zwar die Parasiten in Schach, verursacht aber an anderer Stelle Kollateralschäden. Oder vielleicht verändern die Parasiten, die den Neurotransmitter Dopamin produzieren und mit den Zellen, die sie infizieren, interagieren, das Verhalten ihres Wirts.Wir haben einer führenden Autorität auf dem Gebiet von Toxoplasma gondii und Toxoplasmose, Rima McLeod, MD, Professorin für Augenheilkunde & und Pädiatrie und medizinische Leiterin des Toxoplasmosezentrums an der Universität von Chicago, eine wichtige Frage gestellt: Was passiert wohl, wenn Milliarden von Menschen mit einer parasitären Gehirninfektion durchs Leben gehen?
Zunächst einmal: Was ist Toxoplasma gondii?
Rima McLeod: Toxoplasma gondii ist ein mikroskopisch kleiner Parasit, der mit dem Parasiten verwandt ist, der Malaria verursacht. Er hat mehrere Lebenszyklusstadien.
Es handelt sich um einen Parasiten, der Chancengleichheit bietet. Er infiziert Menschen auf der ganzen Welt, ohne Rücksicht auf Ort, ethnische Zugehörigkeit oder sozioökonomischen Status, obwohl die Genetik des Wirtes eine wichtige Rolle bei den Manifestationen der Infektion spielt.
Und was ist mit Toxoplasmose?
Toxoplasmose bezieht sich auf die durch diesen Parasiten verursachten Krankheiten. Ich sollte Parasiten sagen. Wir lernen, dass sich genetisch unterschiedliche Parasiten in den Krankheiten, die sie verursachen, unterscheiden, oft auch je nach geografischem Standort. So kommen beispielsweise in verschiedenen Klimaregionen der USA unterschiedliche genetische Parasitentypen vor, die unterschiedlich schwere Krankheiten verursachen.
Der Parasit kann in seiner akuten, aktiven Form Krankheiten verursachen, wenn er von älteren Kindern und Erwachsenen erworben wird. Manchmal schädigt er das Auge und gelegentlich Herz oder Gehirn oder verursacht vergrößerte Lymphknoten. Er ist die häufigste infektiöse Ursache für die Zerstörung des Augenhintergrunds. Der Parasit ruht dann, kann aber in seiner aktiven, zerstörerischen Form wieder auftreten, wenn das Immunsystem nicht normal ist, wie z. B. bei Personen mit bösartigen Erkrankungen oder AIDS oder während einer Behandlung, die das Immunsystem unterdrückt. In diesem Fall kann der Parasit das Gehirn oder andere Organe schädigen.
Wenn eine Frau die Infektion zum ersten Mal während ihrer Schwangerschaft erwirbt und den Parasiten auf ihren Fötus überträgt, führt dies zu einer kongenitalen parasitären Infektion. Unbehandelt oder wenn sie zu spät erkannt wird, kann dies eine schreckliche Krankheit sein. In diesem Fall kann sie zum Verlust des Augenlichts, zu schweren Gehirnentzündungen und dauerhaften neurologischen Schäden führen.

Auch wenn bei der Geburt keine schweren Symptome auftreten, kann die Krankheit von der ruhenden in die aktive Phase übergehen und neue Schäden an Auge und Gehirn verursachen. Deshalb ist das Screening auf eine Infektion bei schwangeren Frauen so wichtig.
Wie infizieren sich Menschen?
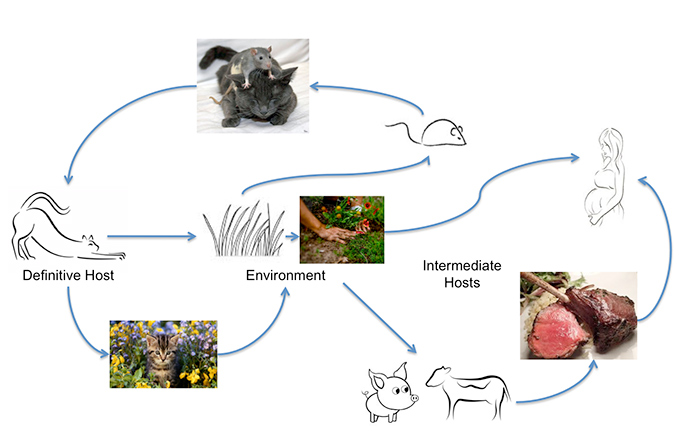
Toxoplasma gondii kann die meisten Warmblüter infizieren, auch den Menschen, aber der Hauptwirt, bei dem ein genetischer Austausch stattfindet, sind Katzen. Der Mensch kann sich durch den Verzehr von unzureichend gegartem Fleisch oder durch die Aufnahme von Oozysten infizieren, die von Katzen ausgeschieden werden, z. B. auf ungewaschenem Gemüse oder aus kontaminiertem Wasser. Ein unerkannter Kontakt mit Oozysten kann leicht passieren, da eine akut infizierte Katze innerhalb von zwei Wochen bis zu 500 Millionen Toxoplasma-Oozysten ausscheiden kann. Schon eine einzige Oozyste ist infektiös. Diese überleben in warmer, feuchter Erde und Wasser ein Jahr lang. Eine Studie der Johns Hopkins University ergab, dass die jährliche Oozystenbelastung, die bei Erhebungen in Gemeinden gemessen wurde, zwischen drei und 434 Oozysten pro Quadratmeter liegt. Diese Zahlen steigen in Gebieten, in denen Katzen selektiv ihren Kot absetzen, erheblich an“, heißt es weiter. Das ist der Grund, warum die Infektion so häufig ist.
OK. Das ist beunruhigend. Was passiert, wenn jemand ein paar Oozysten zu sich nimmt?
T. gondii ist ein obligat intrazellulärer Parasit. Das bedeutet, dass er die Zellen des Wirts infizieren muss, um zu überleben. Die Zellen, in denen er bevorzugt lebt, wenn er sich im Ruhezustand befindet, sind das Gehirn und die Netzhaut im hinteren Teil des Auges. Er infiziert und versteckt sich dann und vermehrt sich langsam in diesen Zellen. Es handelt sich um eine chronische, lebenslange Infektion.
Was passiert mit Menschen, die immunologisch normal sind und vor der Geburt nicht exponiert waren, die sich aber später mit Parasiten infizieren?
Viele Ärzte haben solche latenten oder asymptomatischen Fälle als klinisch unbedeutend angesehen. In meiner Forschungsgruppe und in meinem Labor haben wir uns auf die Biologie aktiver Infektionen konzentriert, insbesondere bei Kindern, und darauf, wie man sie am besten verhindern oder behandeln kann. Seit mehr als einem Jahrzehnt gibt es jedoch zahlreiche Studien über subtile oder auch nicht so subtile Veränderungen im Verhalten von Tieren, die mit einer latenten T. gondii-Infektion in Verbindung stehen. Mäuse und Ratten mit einer Infektion verlieren beispielsweise ihre Abneigung gegen den Geruch von Katzen, insbesondere gegen Katzenurin. Diese so genannte tödliche Anziehungskraft der Katze ist für jedes Nagetier, das durch die Infektion furchtlos geworden ist, gefährlich; sie macht es für Katzen leichter, sie zu fangen und zu fressen. Wir haben festgestellt, dass chronisch infizierte Mäuse zusätzliche Verhaltensänderungen aufweisen, wie z. B. Frieren auf offenem Feld, schlechtere Körperpflege, Verlust des Gleichgewichts und verminderte Griffkraft. Diese Verhaltensweisen sind typisch für eine ungesunde Alterung. Die Gehirne von chronisch infizierten Mäusen sind kleiner als die von normalen Kontrollpersonen. Wir finden Parasiten in Zysten innerhalb von Neuronen, die Synapsen gebildet hatten. Wir sehen auch einen Entzündungsprozess, vor allem in und neben dem Teil des Gehirns, der mit dem Gedächtnis verbunden ist.

Gibt es ein menschliches Äquivalent zu solchen Verhaltensänderungen?
Ich hatte früher meine Zweifel, aber ich bin mir nicht mehr so sicher, dass diese Verhaltensänderung nur Nager betrifft. In einer aktuellen Studie aus Stanford wurden im Blut von chronisch und akut infizierten schwangeren Frauen Veränderungen bei Molekülen des Immunsystems festgestellt, die bei nicht infizierten Kontrollpersonen nicht vorhanden waren. Eine Gruppe an der Johns Hopkins University fand subtile, aber spezifische Gedächtnisdefizite bei jungen Berufstätigen, die Antikörper gegen den Parasiten aufwiesen, im Vergleich zu entsprechenden Kontrollen. Diese Gruppen haben herausgefunden, dass Patienten mit Schizophrenie oder Zwangsstörungen statistisch gesehen mit größerer Wahrscheinlichkeit eine T. gondii-Infektion haben. Infizierte Männer haben eine langsamere Reaktionszeit und mehr als doppelt so viele Verkehrsunfälle. Es gibt auch Zusammenhänge zwischen Antikörpern gegen den Parasiten und bipolaren Erkrankungen, Suizidalität und sogar einer optimistischen Einstellung, die möglicherweise mit den Auswirkungen des Parasiten auf Dopamin zusammenhängen. Eine Analyse aus Frankreich aus dem Jahr 2012, wo schätzungsweise 43 Prozent der Menschen T. gondii in sich tragen, kam zu dem Schluss, dass Männer mit einer latenten Infektion dazu neigen, „dogmatischer, weniger selbstbewusst, eifersüchtiger, weniger impulsiv und ordentlicher zu sein als nicht infizierte Männer. Infizierte Frauen schienen wärmer, gewissenhafter, hartnäckiger, unsicherer und scheinheiliger zu sein.“
Wie misst man Scheinheiligkeit?
Ich weiß nicht, was ich davon halten soll, oder von den vielen Assoziationsstudien, denn es ist schwer zu sagen, was zuerst da war: die Infektion oder das Merkmal. Es gibt einen Wissenschaftler, der sich für ein bodenständiges Beispiel aus erster Hand hält. Der tschechische Forscher Jaroslav Flegr, Professor an der Karlsuniversität in Prag, spricht und schreibt über Veränderungen, die er in seinem eigenen Verhalten festgestellt hat, nachdem er sich mit T. gondii infiziert hatte. Er behauptet, dass latente Toxoplasma-Infektionen bei Männern dazu führen, dass sie sich eher zurückziehen, feindselig oder unsozial werden oder regelrecht „griesgrämig“ sind. Infizierte Frauen hingegen suchen Trost in sozialen Bindungen und in der Fürsorge. Sie neigen dazu, sich zu kümmern und Freundschaften zu schließen. Flegr ist dafür bekannt, dass er sie mit „Sex-Kätzchen“ vergleicht. Fragen Sie mich nicht, was das mit Heiligkeit zu tun hat. Diese Art von Information ist in der Literatur zu finden, aber derzeit nicht definitiv als Ursache und Wirkung bewiesen.
Auch kann griesgrämiges Verhalten schwer zu messen sein, ja?
Genau, deshalb konzentriert sich unser Labor lieber darauf zu verstehen, wie T. gondii ihren Schaden anrichtet, die Gene, die diesen Prozess in Gang setzen, sowie diejenigen, die vor einer Toxoplasma-Infektion schützen. Wir wollen Medikamente zur Heilung entwickeln und einen Impfstoff zur Vorbeugung herstellen. Im Laufe unserer genetischen Studien sind wir jedoch auf zahlreiche Verbindungen zwischen den genetischen Bahnen, die zur Kontrolle der T. gondii-Infektion beitragen, und denjenigen, die bei neurologischen Erkrankungen und Neurodegeneration eine Rolle spielen, gestoßen. Ich habe zunehmend den Verdacht, dass dieser Parasit – durch die Reaktion des Immunsystems auf ihn und die direkten Interaktionen der Parasiten mit neuronalen Stamm- und differenzierten Wirtszellen – dieselben Bahnen beeinflusst, die mit neurologischen Störungen, einschließlich Alzheimer und möglicherweise Autismus, in Verbindung gebracht werden. Und es gibt Hinweise darauf, wie der Parasit bei einigen genetisch anfälligen Menschen, die ihm ausgesetzt sind, zu diesen Krankheiten beitragen könnte.
Wie haben Sie die Verbindung hergestellt?
Wir haben uns die Gene genau angesehen, die am Schutz eines Wirts vor diesem Parasiten beteiligt sind. In einer Studie aus Frankreich aus dem Jahr 2006 wurde eine kleine Region auf dem Rattenchromosom 10 identifiziert, die jetzt Toxo1 genannt wird. Diese Region enthält etwa 30 Gene. Sie fanden heraus, dass einige dieser Gene eine zentrale Rolle bei der Verhinderung der Vermehrung und Ausbreitung des Parasiten in Rattenzellen spielen. Interessanterweise stammten die Gene, die vor Toxo schützen, von Lewis-Ratten, einem normalen, gutmütigen Versuchstier, das seit Generationen im Labor gezüchtet wird. Die Gene, die Toxo nicht verhindern, kommen häufig bei braunen Wanderratten vor, den harten Kerlen, die von vielen als „Kanalisationsratten“ bezeichnet werden. Zu dieser Zeit hatten unsere Kollegen in Frankreich, an den Universitäten in Grenoble und Toulouse, Schwierigkeiten zu bestimmen, welche Gene in dieser Region entscheidend sein könnten. Ihre Arbeit an Ratten veranlasste uns, nach Ähnlichkeiten in der Genregion beim Menschen zu suchen. Dies war der Anstoß für unsere Studien, um eine ähnliche Reihe von Genen, mit einigen signifikanten Unterschieden, auf dem menschlichen Chromosom 17 zu finden. Wir verfolgen etwa 250 Familien – jede umfasst eine Mutter, einen Vater und ein Kind, das in utero mit Toxoplasma infiziert wurde. In etwa 20 dieser Familien haben wir Zwillingspaare, die gemeinsam exponiert waren. In einigen Fällen handelt es sich um eineiige Zwillinge, die beide sehr krank sind und die gleichen Infektionserscheinungen aufweisen. In anderen Fällen sind die Symptome minimal. Bei nicht eineiigen Zwillingen ist manchmal einer der beiden schwer erkrankt, während der andere normal erscheint. Wir wissen also, dass die Vererbung von schützenden oder anfälligen Genvarianten von Mutter und Vater einen Unterschied ausmachen kann. Wir schauen uns jetzt jedes dieser und weitere Gene genau an.
Was bewirken diese Gene und was haben Sie gelernt?Wir haben gerade eine Arbeit über ALOX12 in der Zeitschrift Infection and Immunity veröffentlicht. Wir stehen noch am Anfang der Untersuchung aller Gene, aber die bisherigen Ergebnisse sind faszinierend. Wir haben einen Kandidatengen-Ansatz verwendet. Die ersten beiden von uns untersuchten Gene, eines an beiden Enden der Toxo1-Region, wiesen Variationen auf, die in hohem Maße mit Anfälligkeit oder Resistenz korrelieren. Zuvor hatten wir dies bei dem Gen am unteren Ende der Region festgestellt, das damals als Raupe bezeichnet wurde. In der aktuellen Arbeit haben wir es in einem Gen am oberen Ende der Region gefunden, das ALOX12 heißt. Dabei handelt es sich um ein Zelltod-Gen.
Technisch gesehen handelt es sich um eine Lipoxygenase, die einen giftigen, instabilen Sauerstoff an den zwölften Kohlenstoff der Arachidonsäure anhängt, wodurch ein biologisch schädliches Molekül entsteht. Als wir Variationen dieses Gens von verschiedenen Eltern und Kindern untersuchten, stellten wir fest, dass sich bestimmte Allele – spezielle Variationen von vier Teilen des Gens – signifikant unterschieden und dass diese Unterschiede mit der Anfälligkeit verbunden waren. Wenn wir ALOX12 reduzierten, nahmen die entzündlichen und zelltötenden Aktivitäten, die vor Toxoplasmose schützen, ab. Es ist wahrscheinlich, dass bestimmte Varianten dieses Gens bei der Auslösung von Entzündungen und der Abtötung von infizierten und benachbarten Zellen und Parasiten effektiver sind als andere. Mit dem Enzymprodukt dieses Gens konnte die Infektion besser in den menschlichen Zellen eingedämmt werden. Ohne das Produkt dieses Gens waren die gleichen Zellen nicht in der Lage, die Infektion einzudämmen. Als wir diese Zellen testeten, bei denen das ALOX12-Gen inaktiviert war, vermehrten sich die Parasiten schnell.
Das andere Gen am anderen Ende der Region, bekannt als Caterpillar oder NALP1, hatte eine ähnliche Wirkung. Wir haben dies 2011 veröffentlicht.
Gibt es eine Kehrseite dieser aggressiven Anti-Parasiten-Gene?
Diese Zelltod-Faktoren, die in diesem kritischen Gencluster namens Toxo1 zu finden sind, sind wichtig, um diese Infektion zu begrenzen. Aber wir vermuten jetzt, dass eine hohe Aktivität dieser Gene im späteren Leben eine schädliche Wirkung haben könnte, indem sie nicht nur die Wirtszellen der Parasiten, sondern auch unschuldige Umstehende töten. Dies ist eine Vermutung, aber sie könnte erklären, warum ein Genpolymorphismus, der beim Auftreten von Alterskrankheiten eine Rolle zu spielen scheint, von der Evolution dennoch bevorzugt wird, weil er eine häufige Infektion im frühen Leben, insbesondere bis zum gebärfähigen Alter, verhindern oder kontrollieren kann.
Warum sollten diese Gene ihre Auswirkungen auf das Verhalten oder neurologische Erkrankungen konzentrieren?
Toxoplasma infiziert Nervenzellen. Bestimmte Versionen von ALOX12 und NALP1 können dazu beitragen, dass eine infizierte Person eine starke, frühzeitige, schützende Immunreaktion auslöst, die Parasiten, infizierte Zellen sowie Zellen in der Nähe abtötet. Wir wissen aber auch, dass ALOX12 mit Krankheiten im Zusammenhang mit Alterung und Gedächtnisverlust in Verbindung gebracht wird. Als wir unsere Erkenntnisse über ALOX12 mit systembiologischen Programmen nutzten, die zur Kartierung von Signalwegen eingesetzt werden, erkannten wir, dass viele dieser Signalwege auch bei verschiedenen neurodegenerativen Krankheiten wie Alzheimer und sogar Schizophrenie eine Rolle spielen. Einige tragen möglicherweise zu Arteriosklerose oder Diabetes bei. Wirksamere Medikamente oder ein Impfstoff könnten vor den verheerenden Krankheiten schützen, die dieser Parasit verursacht. Diese neue Arbeit eröffnet die Möglichkeit, dass bessere Behandlungen, die die Infektion schnell unter Kontrolle bringen oder beseitigen, auch die altersbedingten Krankheiten reduzieren könnten, die wir bei einigen Menschen mit Toxoplasma in Verbindung bringen.
Das ist ein großes Projekt.
Es war eine wunderbare Zusammenarbeit mit Kollegen in Frankreich, England und Kanada und einem Team an der Universität von Kansas, zusammen mit der Arbeit einer bemerkenswerten Gruppe junger Wissenschaftler in meinem eigenen Labor.

Das ist ermutigend. Mit wem arbeiten Sie zusammen, um diese Entdeckung voranzutreiben?
Wir arbeiten im Rahmen unserer eigenen Forschungsprogramme und Laborgruppe sowie mit Kollegen in New Haven, dem J Craig Ventner Institute und dem Institute for Systems Biology in Seattle sowie einer Reihe anderer Kollegen zusammen. Wir freuen uns sehr über die Erkenntnisse und das Potenzial, die Prävention und Behandlung durch diese Arbeit voranzubringen.