
Téměř třetina ze 7,25 miliardy lidí na Zemi, včetně přibližně 60 milionů lidí ve Spojených státech, je chronicky infikována protozoem Toxoplasma gondii. Fungující imunitní systém dokáže udržet parazita na uzdě, takže pouze menšina nakažených má výrazné příznaky. Když se však nic netušící žena nakazí během těhotenství a předá parazita svému nenarozenému dítěti, následky mohou být hluboké.
Mezi ně patří devastující poškození mozku, nervového systému a očí. Nyní přibývá důkazů, že někteří lidé, možná mnoho lidí, mají jemnější příznaky vyvolané infekcí. Možná, že imunitní reakce sice drží parazity pod kontrolou, ale způsobuje vedlejší škody jinde. Nebo možná paraziti, kteří produkují neurotransmiter dopamin a interagují s buňkami, které infikují, modifikují chování svého hostitele. na velkou otázku jsme se zeptali přední odbornice na Toxoplasma gondii a toxoplazmózu, doktorky Rimy McLeodové, profesorky oftalmologie & zrakových věd a pediatrie a lékařské ředitelky centra pro toxoplazmózu na Chicagské univerzitě: Pro začátek, co je to Toxoplasma gondii?
Rima McLeod: Toxoplasma gondii je mikroskopický parazit příbuzný parazitovi, který způsobuje malárii. Má několik stadií životního cyklu.
Jedná se o parazita s rovnými příležitostmi. Infikuje osoby po celém světě bez ohledu na místo, etnickou příslušnost nebo socioekonomický status, i když genetika hostitele hraje důležitou roli v projevech infekce.
A co toxoplazmóza?
Toxoplazmóza označuje onemocnění způsobená tímto parazitem. Měl bych říci parazitů. Zjišťujeme, že geneticky odlišní parazité se liší v nemocech, které způsobují, často se liší podle zeměpisné polohy. Například v různých klimatických oblastech USA se vyskytují různé genetické typy parazitů, které způsobují různě závažná onemocnění.
Parazit může způsobit onemocnění v akutní, aktivní formě, pokud se jím nakazí starší děti a dospělí. Někdy poškozuje oko a příležitostně srdce nebo mozek nebo způsobuje zvětšení lymfatických uzlin. Je nejčastější infekční příčinou destrukce očního pozadí. Poté se stává neaktivní, ale může znovu propuknout ve své aktivní destruktivní formě, pokud imunitní systém není normální, například u osob se zhoubnými nádory nebo AIDS nebo během léčby, která potlačuje imunitní systém. V takovém případě může parazit poškodit mozek nebo jiné orgány.
Pokud se žena nakazí poprvé v těhotenství a přenese parazita na svůj plod, vzniká vrozená parazitární infekce. Pokud není léčena nebo je zachycena příliš pozdě, může se jednat o strašlivé onemocnění. V takovém případě může způsobit ztrátu zraku, těžký zánět mozku a trvalé neurologické poškození.

I když se při porodu nevyskytují závažné příznaky, může přejít z klidové fáze do aktivní a způsobit nové poškození oka a mozku. Proto je tak důležitý screening infekce u těhotných žen.
Jak se lidé nakazí?
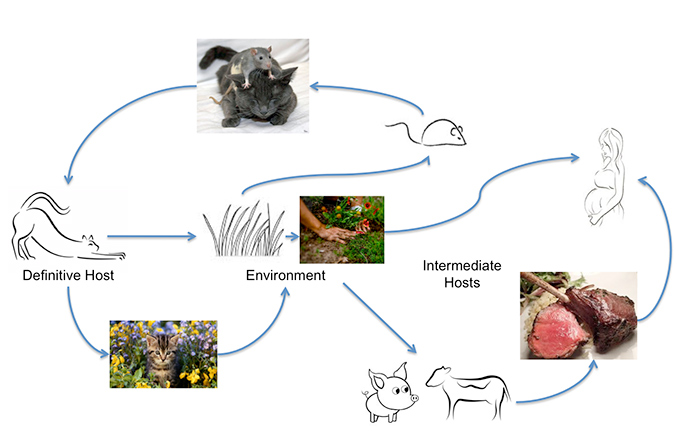
Toxoplasma gondii může infikovat většinu teplokrevných zvířat včetně člověka, ale hlavním hostitelem, u kterého dochází ke genetické výměně, jsou kočky. Lidé se mohou nakazit konzumací nedostatečně tepelně upraveného masa nebo pozřením oocyst vylučovaných kočkami, například na neumyté zelenině nebo z kontaminované vody. K nerozpoznanému kontaktu s oocystami může dojít snadno, protože akutně infikovaná kočka může během dvou týdnů vyloučit až 500 milionů oocyst Toxoplasmy. I jedna oocysta je infekční. Ty přežívají v teplé vlhké půdě a vodě po dobu jednoho roku. Studie Univerzity Johnse Hopkinse zjistila, že roční zátěž oocystami měřená při průzkumech v komunitě je tři až 434 oocyst na čtvereční stopu. Dodávají, že tato čísla se výrazně zvyšují „v oblastech, kde kočky selektivně kálí“. Proto je infekce tak častá.
OK. To je znepokojující. Co se stane, když někdo pozře několik oocyst?
T. gondii je obligátně intracelulární parazit. To znamená, že musí infikovat buňky hostitele, aby přežil. Buňky, ve kterých nejraději žije, když je v klidovém stádiu, jsou v mozku a sítnici v zadní části oka. V těchto buňkách se infikuje a pak se v nich pomalu ukrývá a replikuje. Jedná se o chronickou, celoživotní infekci.
Co se stane s lidmi, kteří jsou imunologicky normální a nebyli vystaveni infekci před narozením, kteří se parazitů chytí později?
Mnozí lékaři považovali takové latentní nebo asymptomatické případy za klinicky nevýznamné. V mé výzkumné skupině a laboratoři jsme se zaměřili na biologii aktivních infekcí, zejména u dětí, a na to, jak jim nejlépe předcházet nebo je léčit. Již více než deset let však existuje řada studií jemných nebo ne tak jemných změn v chování zvířat spojených s latentní infekcí T. gondii. Myši a potkani s infekcí například ztrácejí odpor k pachu koček, zejména ke kočičí moči. Tato tzv. fatální kočičí přitažlivost je nebezpečná pro všechny hlodavce, kteří se v důsledku infekce stali nebojácnými; kočky je pak snáze chytí a sežerou. Prospívá však kočkám, které tak získávají snadnou potravu, a pomáhá parazitům, kteří tak získávají nový rezervoár. zjistili jsme, že u chronicky infikovaných myší dochází k dalším změnám chování, jako je zamrzání v otevřeném poli, horší péče o sebe, ztráta rovnováhy a snížená síla úchopu. Toto chování je typické pro nezdravé stárnutí. Mozek chronicky infikovaných myší je menší než mozek normálních kontrol. Parazity nacházíme v cystách uvnitř neuronů, které vytvořily synapse. Vidíme také zánětlivý proces, zejména uvnitř a vedle části mozku spojené s pamětí.

Existuje u člověka ekvivalent takových změn chování?
Dříve jsem měl pochybnosti, ale už si nejsem tak jistý, že se tato změna chování týká pouze hlodavců. Nedávná studie ze Stanfordu prokázala změny molekul imunitního systému v krvi chronicky a akutně infikovaných těhotných žen, které nebyly přítomny u nenakažených odpovídajících kontrol. Skupina z Johns Hopkins University zjistila u mladých profesionálů, kteří měli protilátky proti parazitovi, jemné, ale specifické poruchy paměti ve srovnání s odpovídajícími kontrolami. několik výzkumných týmů hledalo vliv na osobnost nebo chování u lidí. Tyto skupiny zjistily, že pacienti se schizofrenií nebo obsedantně-kompulzivní poruchou mají statisticky vyšší pravděpodobnost infekce T. gondii. Nakažení muži mají pomalejší reakční dobu a více než dvakrát častější dopravní nehody. Existují také asociace výskytu protilátek proti tomuto parazitovi s bipolárním onemocněním, sebevražedným chováním, dokonce i optimistickou náladou, což pravděpodobně souvisí s účinky parazita na dopamin. Analýza z Francie z roku 2012, kde je podle odhadů nositelem T. gondii 43 % lidí, dospěla k závěru, že muži s latentní infekcí bývají „dogmatičtější, méně sebevědomí, žárlivější, méně impulzivní a spořádanější než nenakažení muži. Nakažené ženy se zdály být vřelejší, svědomitější, vytrvalejší, nejistější a svatouškovitější.“
Jak se měří svatouškovství?“
Nevím, co si o tom mám myslet, ani o mnoha asociačních studiích, protože je těžké zjistit, co bylo dřív: infekce nebo vlastnost. Existuje jeden vědec, který se domnívá, že je přízemním příkladem první osoby. Český vědec Jaroslav Flegr, profesor Univerzity Karlovy v Praze, hovoří a píše o změnách, které zaznamenal ve svém chování poté, co se nakazil T. gondii. Tvrdí, že latentní infekce Toxoplasmou způsobila, že se muži častěji uzavírají do sebe, stávají se nepřátelskými nebo asociálními či přímo „zakřiknutými“. Naopak infikované ženy hledají útěchu prostřednictvím sociálních vazeb a péče. Mají sklon k náklonnosti a přátelství. Flegr je známý tím, že je přirovnává k „sexuálním koťatům“. Neptejte se mě, jak to souvisí se svatouškovstvím. Tento typ informací se v literatuře vyskytuje, ale v současné době není definitivně prokázán jako příčina a následek.
Znovu říkám, že chování kudlanek se dá těžko měřit, že?
Přesně tak, takže naše laboratoř se raději zaměřuje na pochopení toho, jak T. gondii působí škody, na geny, které tento proces iniciují, a také na ty, které chrání před infekcí Toxoplasmou. Chceme vyvinout léky, které by ji léčily, a vakcínu, která by jí zabránila. Naším dlouhodobým cílem je porozumět tomuto onemocnění, abychom mohli zlepšit léčbu a její výsledky. v průběhu našich genetických studií jsme však narazili na četné souvislosti mezi genetickými cestami, které pomáhají řídit infekci T. gondii, a cestami, které se podílejí na neurobehaviorálních onemocněních a neurodegeneraci. Mám stále větší podezření, že tento parazit prostřednictvím reakce imunitního systému na něj a přímých interakcí parazitů s neuronálními kmenovými a diferencovanými buňkami hostitele ovlivňuje stejné dráhy jako dráhy spojené s neurologickými poruchami, včetně Alzheimerovy choroby a možná i autismu. A ukazuje na vodítka, jak by mohl parazit přispívat k těmto onemocněním u některých geneticky náchylných lidí, kteří jsou jim vystaveni.
Jak jste na tuto souvislost přišli?
Podívali jsme se blíže na geny, které se podílejí na ochraně hostitele před tímto parazitem. Studie z Francie z roku 2006 identifikovala malou oblast na krysím chromozomu 10, která se nyní nazývá Toxo1. Tato oblast obsahuje přibližně 30 genů. Zjistili, že některé z těchto genů hrají ústřední roli v prevenci množení a šíření parazita v buňkách potkana. Zajímavé je, že geny, které chrání proti Toxo, pocházejí z Lewisových potkanů, standardních, učenlivých pokusných zvířat chovaných po generace v laboratoři. Geny, které nedokážou zabránit Toxo, jsou běžné u hnědých norských potkanů, drsňáků, kterým mnozí lidé říkají „kanálové krysy.“ V té době měli naši kolegové ve Francii, na univerzitách v Grenoblu a Toulouse, potíže s určením, které geny v této oblasti by mohly být klíčové. Jejich práce na krysách nás vedla k hledání podobností v této genové oblasti u lidí. To odstartovalo naše studie, jejichž cílem bylo vystopovat podobný soubor genů s některými významnými rozdíly na lidském chromozomu 17. Desítky let práce s pacienty nám daly obrovský náskok. Sledujeme asi 250 rodin – každá zahrnuje matku, otce a dítě nakažené Toxoplasmou v děloze. Přibližně ve 20 z těchto rodin máme sady dvojčat, která byla exponována společně. V některých případech máme jednovaječná dvojčata, obě velmi nemocná, se stejnými projevy infekce. V jiných případech jsou příznaky minimální. V případech, kdy se jedná o neidentická dvojčata, je někdy jedno z dvojice hluboce postižené a druhé se zdá být normální. Víme tedy, že dědičnost ochranných nebo náchylnostních variant genů po matce a otci může mít vliv. Každý z těchto a dalších genů nyní podrobně zkoumáme.
Co tyto geny dělají a co jste se dozvěděli?Právě jsme publikovali článek o genu ALOX12 v časopise Infection and Immunity. Jsme na začátku procesu zkoumání všech genů, ale dosavadní výsledky jsou fascinující. Použili jsme přístup kandidátních genů. První dva geny, které jsme zkoumali, jeden z obou konců oblasti Toxo1, měly odchylky, které na vysoké úrovni korelují buď s vnímavostí, nebo s odolností. Již dříve jsme to zjistili u genu v dolní části oblasti, tehdy známého jako caterpillar. V této aktuální práci jsme to našli v genu v horní části oblasti, který se nazývá ALOX12. Jedná se o gen buněčné smrti.
Technicky se jedná o lipoxygenázu, která přidává toxický, nestabilní kyslík ke 12. uhlíku kyseliny arachidonové – vytváří biologicky škodlivou molekulu. Jiní našli důkazy o tom, že ALOX12 ovlivňuje výsledky u cukrovky, neurodegenerativních onemocnění a schizofrenie, ale o jeho roli u infekčních onemocnění nebylo nic známo. když jsme testovali varianty tohoto genu od různých rodičů a dětí, zjistili jsme, že některé alely – konkrétní varianty čtyř částí genu – se významně liší a že tyto rozdíly souvisejí s náchylností. Když jsme ALOX12 snížili, snížila se zánětlivá aktivita a aktivita odumírání buněk, které chrání před toxoplazmózou. Ukázalo se, že některé varianty tohoto genu jsou při spouštění zánětu a zabíjení infikovaných a blízkých buněk a parazitů účinnější než jiné. U enzymového produktu tohoto genu došlo k silnějšímu účinku při udržování infekce v lidských buňkách. Bez produktu tohoto genu nebyly tytéž buňky schopny infekci omezit. Když jsme tyto buňky testovali s neaktivním genem ALOX12, parazité se rychle množili. podobný účinek měl i druhý gen na druhém konci oblasti, známý jako caterpillar neboli NALP1. To jsme publikovali v roce 2011.
Mají tyto agresivní antiparazitární geny nějakou stinnou stránku?
Tyto faktory buněčné smrti, které se nacházejí v tomto kritickém shluku genů zvaném Toxo1, jsou důležité pro omezení této infekce. Nyní však máme podezření, že vysoká aktivita těchto genů v pozdějším věku může mít škodlivý účinek a zabíjet nejen hostitelské buňky parazitů, ale i nevinné kolemjdoucí. Je to sice jen domněnka, ale mohla by pomoci vysvětlit, proč genový polymorfismus, který podle všeho hraje roli při vzniku nemocí spojených se stárnutím, může být přesto evolucí upřednostňován pro svou schopnost zabránit nebo kontrolovat běžnou infekci v časném životě, zejména až do reprodukčního věku.
Proč by se tyto geny zaměřovaly svým účinkem na chování nebo neurologická onemocnění?
Toxoplasma infikuje nervové buňky. Určité verze ALOX12 a NALP1 mohou pomoci infikované osobě vytvořit silnou, časnou, ochrannou imunitní odpověď, která zabíjí parazity, infikované buňky i buňky v okolí. Víme však také, že ALOX12 je spojen s nemocemi souvisejícími se stárnutím a ztrátou paměti. Když jsme naše poznatky o ALOX12 využili pomocí programů systémové biologie, které se používají k mapování drah, uvědomili jsme si, že mnohé z těchto drah jsou ve hře také u různých neurodegenerativních onemocnění, jako je Alzheimerova choroba a dokonce schizofrenie. Některé mohou přispívat k ateroskleróze nebo cukrovce. Když tato silná imunitní reakce zůstane v práci, může mít účinky, které mohou být škodlivé. účinnější léky nebo vakcína by mohly chránit před ničivými nemocemi, které tento parazit způsobuje. Tato nedávná práce zvyšuje možnost, že lepší léčba rychlým zvládnutím nebo odstraněním infekce může u některých lidí omezit i nemoci související s věkem, o nichž spekulujeme, že mohou být spojeny s toxoplasmou.
Je to velký projekt. Zdá se, že v tomto úsilí máte mnoho partnerů, že?“
Jedná se o úžasnou spolupráci s kolegy ve Francii, Anglii a Kanadě a týmem na Kansaské univerzitě, spolu s prací pozoruhodné skupiny mladých vědců v mé vlastní laboratoři.

To je povzbudivé. S kým spolupracujete, abyste tento objev posunuli dál?
Spolupracujeme v rámci našich vlastních výzkumných programů a laboratorní skupiny a s kolegy v New Havenu, v Institutu J. Craiga Ventnera a v Institutu pro systémovou biologii v Seattlu a s řadou dalších kolegů. Jsme velmi nadšeni poznatky a potenciálem pro pokrok v prevenci a léčbě, které tato práce přináší.
.