
Næsten en tredjedel af de 7,25 milliarder mennesker på jorden, herunder anslået 60 millioner mennesker i USA, er kronisk smittet med protozoen Toxoplasma gondii. Et fungerende immunsystem kan holde parasitten i skak, så kun et mindretal af de smittede har væsentlige symptomer. Men når en intetanende kvinde bliver smittet under graviditeten og giver parasitten videre til sit ufødte barn, kan konsekvenserne være alvorlige.
De omfatter ødelæggende skader på hjernen, nervesystemet og øjnene. Nu er der voksende beviser for, at nogle mennesker, måske mange mennesker, har mere subtile symptomer, der udløses af infektionen. Måske forårsager immunreaktionen, mens den holder parasitterne i skak, kollaterale skader andre steder. Eller måske ændrer parasitterne, som producerer neurotransmitteren dopamin og interagerer med de celler, de inficerer, værtens adfærd.Vi stillede en førende autoritet inden for Toxoplasma gondii og toxoplasmose, Rima McLeod, MD, professor i oftalmologi & synsvidenskab og pædiatri og medicinsk direktør for toxoplasmosecentret ved University of Chicago, et stort spørgsmål: Hvad tror vi, der sker, når milliarder af mennesker går gennem livet med en parasitær hjerneinfektion?
For at starte med, hvad er Toxoplasma gondii?
Rima McLeod: Toxoplasma gondii er en mikroskopisk parasit, der er beslægtet med den parasit, der forårsager malaria. Den har flere livscyklusstadier.
Det er en parasit med lige muligheder for alle. Den inficerer personer over hele verden uden respekt for sted, etnicitet eller socioøkonomisk status, selv om værtsgenetik spiller en vigtig rolle for infektionens manifestationer.
Og hvad med toxoplasmose?
Toxoplasmose henviser til de sygdomme, der forårsages af denne parasit. Jeg burde sige parasitter. Vi er ved at lære, at genetisk forskellige parasitter adskiller sig fra hinanden med hensyn til de sygdomme, de forårsager, og at de ofte varierer alt efter geografisk placering. F.eks. findes der forskellige genetiske typer parasitter i forskellige klimaregioner i USA, som forårsager forskellige sværhedsgrader af sygdom.
Parasitten kan forårsage sygdom i sin akutte, aktive form, når den erhverves af ældre børn og voksne. Nogle gange beskadiger den øjet og lejlighedsvis hjertet eller hjernen eller forårsager forstørrede lymfeknuder. Det er den mest almindelige infektiøse årsag til ødelæggelse af øjenryggen. Den går derefter i dvale, men kan genopstå i sin aktive, ødelæggende form, når immunsystemet ikke er normalt, f.eks. hos personer med maligniteter eller AIDS eller under behandling, der undertrykker immunsystemet. I så fald kan parasitten skade hjernen eller andre organer.
Når en kvinde får infektionen for første gang, mens hun er gravid, og overfører parasitten til sit foster, medfører dette en medfødt parasitinfektion. Det kan være en frygtelig sygdom, når den ikke behandles eller opdages for sent. I den situation kan den forårsage tab af synet, alvorlig hjernebetændelse og permanente neurologiske skader.

Selv når der ikke er alvorlige symptomer ved fødslen, kan det skifte fra den hvilende til den aktive fase og forårsage nye skader på øjet og hjernen. Derfor er det så vigtigt at screene gravide kvinder for infektion.
Hvordan får mennesker infektionen?
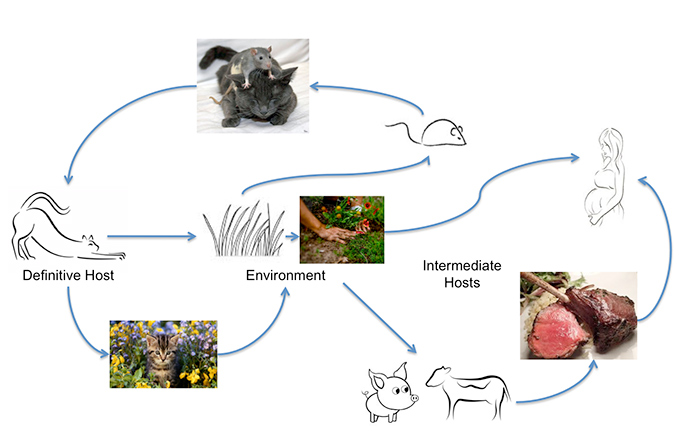
Toxoplasma gondii kan smitte de fleste varmblodede dyr, herunder mennesker, men den primære vært, hvor der sker genetisk udveksling, er katte. Mennesker kan få infektionen ved at spise utilstrækkeligt tilberedt kød eller ved at indtage oocyster, der udskilles af katte, f.eks. på uvaskede grøntsager eller fra forurenet vand. Ukendt kontakt med oocyster kan let ske, da en akut inficeret kat kan udskille op til 500 millioner Toxoplasma-oocyster på to uger. Selv én oocyst er smitsom. Disse overlever i varm fugtig jord og vand i et år. En undersøgelse fra Johns Hopkins University viste, at den årlige oocystebyrde, der er målt i samfundsundersøgelser, er mellem 3 og 434 oocyster pr. kvadratmeter. De tilføjer, at disse tal stiger meget, “i områder, hvor katte selektivt aflægger afføring”. Det er derfor, at infektionen er så almindelig.
OK. Det er foruroligende. Hvad sker der, når nogen indtager et par oocyster?
T. gondii er en obligat intracellulær parasit. Det betyder, at den skal inficere værtens celler for at overleve. De celler, som den foretrækker at leve i, når den er i sit hvilende stadium, er i hjernen og nethinden, bag i øjet. Den inficerer, og derefter gemmer den sig og formerer sig langsomt i disse celler. Det er en kronisk, livslang infektion.
Hvad sker der med mennesker, der er immunologisk normale og ikke blev udsat før fødslen, men som senere får parasitter?
Mange læger har betragtet sådanne latente eller asymptomatiske tilfælde som klinisk ubetydelige. I min forskningsgruppe og mit laboratorium har vi fokuseret på biologien bag aktive infektioner, især hos børn, og hvordan man bedst kan forebygge eller behandle dem. I mere end et årti har der imidlertid været adskillige undersøgelser af subtile, eller ikke så subtile, ændringer i dyreadfærd i forbindelse med latent T. gondii-infektion. Mus og rotter med en infektion mister f.eks. deres aversion mod lugten af katte, især mod katteurin. Denne såkaldte fatale tiltrækning fra katte er farlig for alle gnavere, der er blevet frygtløse af infektionen; det gør det lettere for katte at fange og spise dem. Men det er til gavn for kattene, som får et let måltid, og det er til gavn for parasitterne, som får et nyt reservoir.Vi fandt ud af, at kronisk inficerede mus har yderligere adfærdsændringer, såsom at de fryser i en åben mark, at de plejer sig selv dårligere, at de mister balancen og har nedsat grebsstyrke. Disse adfærdsmønstre er typiske for usund aldring. Hjerner fra kronisk inficerede mus er mindre end hjerner fra normale kontroller. Vi finder parasitter i cyster i neuroner, der havde dannet synapser. Vi ser også en inflammatorisk proces, især inden for og ved siden af den del af hjernen, der er forbundet med hukommelse.

Er der en menneskelig pendant til sådanne adfærdsændringer?
Jeg plejede at have mine tvivl, men jeg er ikke længere så sikker på, at denne adfærdsændring kun involverer gnavere. En nyere undersøgelse fra Stanford viste ændringer i immunsystemets molekyler i blodet fra kronisk og akut inficerede gravide kvinder, som ikke var til stede i ikke-inficerede matchede kontroller. En gruppe fra Johns Hopkins University fandt subtile, men specifikke hukommelsesunderskud hos unge fagfolk, der havde antistoffer mod parasitten, sammenlignet med matchede kontroller.Flere forskergrupper har undersøgt virkningerne på personlighed eller adfærd hos mennesker. Disse grupper har fundet ud af, at patienter med skizofreni eller obsessiv-kompulsiv lidelse statistisk set har større sandsynlighed for at have en T. gondii-infektion. Inficerede mænd har langsommere reaktionstider og mere end dobbelt så mange trafikulykker. Der er også forbindelser mellem at have antistoffer mod parasitten og bipolar sygdom, selvmordsadfærd og endda en optimistisk indstilling, hvilket muligvis hænger sammen med parasittens virkninger på dopamin. En analyse fra 2012 fra Frankrig, hvor anslået 43 procent af befolkningen bærer T. gondii, konkluderede, at mænd med en latent infektion har en tendens til at være “mere dogmatiske, mindre selvsikre, mere jaloux, mindre impulsive og mere ordholdende end ikke-inficerede mænd. Inficerede kvinder virkede varmere, mere samvittighedsfulde, mere vedholdende, mere usikre og mere skinhellige.”
Hvordan måler man skinhellighed?
Jeg ved ikke, hvad jeg skal mene om det, eller om de mange associationsundersøgelser, fordi det er svært at vide, hvad der kom først: infektionen eller egenskaben. Der er en videnskabsmand, der mener, at han er et jordnært førstepersonseksempel. Den tjekkiske forsker Jaroslav Flegr, professor ved Karlsuniversitetet i Prag, taler og skriver om de ændringer, han bemærkede i sin egen adfærd, efter at han fik en T. gondii-infektion. Han har hævdet, at latente Toxoplasma-infektioner gjorde mænd mere tilbøjelige til at trække sig tilbage, til at blive fjendtlige eller asociale eller ligefrem “curmudgeonly”. Inficerede kvinder søger derimod trøst gennem sociale bånd og omsorg. De er tilbøjelige til at pleje og være venner. Flegr har været kendt for at sammenligne dem med “sexkillinger”. Spørg mig ikke, hvordan det hænger sammen med helligbrøde. Denne type oplysninger findes i litteraturen, men er ikke endeligt bevist som en årsag og virkning på nuværende tidspunkt.
Opnå, krumspringende adfærd kan være vanskelig at måle, ikke sandt?
Helt præcist, så vores laboratorium foretrækker at fokusere på at forstå, hvordan T. gondii gør deres skade, de gener, der sætter denne proces i gang, samt de gener, der beskytter mod Toxoplasma-infektion. Vi ønsker at udvikle medicin til at helbrede den og at lave en vaccine til at forebygge den. Vores langsigtede mål har været at forstå denne sygdom for at forbedre behandlingen og resultaterne. i forbindelse med vores genetiske undersøgelser er vi imidlertid stødt på flere forbindelser mellem de genetiske veje, der hjælper med at kontrollere T. gondii-infektion, og dem, der er involveret i neuroadfærdssygdomme og neurodegeneration. Jeg har i stigende grad mistanke om, at denne parasit – via immunsystemets reaktion på den og parasitternes direkte interaktioner med værtens neuronale stamceller og differentierede celler – påvirker de samme veje som dem, der er forbundet med neurologiske sygdomme, herunder Alzheimers sygdom og muligvis autisme. Og det peger på spor om, hvordan parasitten kan bidrage til disse sygdomme for nogle genetisk modtagelige mennesker, der er udsat for dem.
Hvordan fandt I frem til forbindelsen?
Vi kiggede nøje på de gener, der er involveret i at beskytte en vært mod denne parasit. En undersøgelse fra Frankrig fra 2006 identificerede et lille område på rottekromosom 10, som nu kaldes Toxo1. Denne region indeholder omkring 30 gener. De fandt ud af, at nogle af disse gener spiller en central rolle for at forhindre parasittens spredning og spredning i rotteceller. Mærkeligt nok stammer de gener, der beskytter mod Toxo, fra Lewis-rotter, et standardiseret, føjeligt forsøgsdyr, der i generationer er blevet opdrættet i laboratoriet. De gener, der ikke forhindrer Toxo, er almindelige hos brune rotter, de hårde drenge, som mange kalder “kloakrotter”. På det tidspunkt havde vores kolleger i Frankrig, på universiteterne i Grenoble og Toulouse, problemer med at finde ud af, hvilke gener i området der kunne være afgørende i denne sammenhæng. Deres arbejde med rotterne fik os til at kigge efter ligheder i genregionen hos mennesker. Dette satte gang i vores undersøgelser for at spore et lignende sæt gener, med nogle væsentlige forskelle, til det menneskelige kromosom 17. Vores årtiers arbejde med patienter gav os et stort forspring. Vi følger omkring 250 familier – hver familie omfatter en mor, en far og et barn, der er smittet med Toxoplasma in utero. I omkring 20 af disse familier har vi tvillinger, som blev udsat sammen. I nogle tilfælde har vi enæggede tvillinger, der begge er meget syge og har de samme manifestationer af infektion. I andre tilfælde er symptomerne minimale. I tilfælde, hvor der er tale om ikke-identiske tvillinger, er den ene af parrene undertiden dybt påvirket, mens den anden virker normal. Vi ved altså, at det kan gøre en forskel, om man arver beskyttelses- eller modtagelighedsgenvarianter fra mor og far. Vi undersøger nu nøje hvert af disse og andre gener.
Hvad gør disse gener, og hvad har I lært?Vi har netop offentliggjort en artikel om ALOX12 i tidsskriftet Infection and Immunity. Vi er tidligt i processen med at studere alle generne, men resultaterne indtil videre er fascinerende. Vi har anvendt en kandidatgenmetode. De første to gener, vi undersøgte, et fra hver ende af Toxo1-regionen, havde variationer, der på et højt niveau korrelerer med enten modtagelighed eller resistens. Tidligere havde vi fundet dette i genet i bunden af regionen, der dengang var kendt som caterpillar. I denne aktuelle artikel fandt vi det i et gen i toppen af regionen, kaldet ALOX12. Dette er et celledødsgen.
Teknisk set er det en lipoxygenase, der tilføjer en giftig, ustabil ilt til det 12. kulstof i arachidonsyre, hvorved der skabes et biologisk skadeligt molekyle. Andre havde fundet beviser for, at ALOX12 påvirker resultaterne i diabetes, neurodegenerative sygdomme og skizofreni, men der var intet kendt om dets rolle i infektionssygdomme. da vi testede variationer af dette gen fra forskellige forældre og børn, fandt vi, at visse alleler – særlige variationer af fire dele af genet – var signifikant forskellige, og at disse forskelle var forbundet med modtagelighed. Når vi reducerede ALOX12, faldt de inflammatoriske og celledøende aktiviteter, der beskytter mod toxoplasmose. Det blev sandsynligt, at visse varianter af dette gen var mere effektive end andre til at udløse inflammation og dræbe inficerede og nærliggende celler og parasitter. Med enzymproduktet fra dette gen var der en stærkere virkning med hensyn til at holde infektionen indesluttet i menneskelige celler. Uden produktet af dette gen var de samme celler ikke i stand til at holde infektionen tilbage. Når vi testede disse celler med ALOX12-genet gjort inaktivt, spredte parasitterne sig hurtigt. det andet gen i den anden ende af regionen, kendt som caterpillar eller NALP1, havde en lignende virkning. Vi offentliggjorde dette i 2011.
Er der en ulempe ved disse aggressive antiparasitgener?
Disse celledødsfaktorer, der findes i denne kritiske klynge af gener kaldet Toxo1, er vigtige for begrænsningen af denne infektion. Men vi har nu mistanke om, at en høj aktivitet af disse gener senere i livet kan have en skadelig virkning, idet de ikke blot dræber parasitternes værtsceller, men også uskyldige forbipasserende. Dette er en formodning, men det kunne være med til at forklare, hvorfor en genpolymorfisme, der ser ud til at spille en rolle i begyndelsen af sygdomme i forbindelse med aldring, måske stadig foretrækkes af evolutionen for dens evne til at forhindre eller kontrollere en almindelig infektion tidligt i livet, især op til den fødedygtige alder.
Hvorfor skulle disse gener fokusere deres virkninger på adfærd eller neurologiske sygdomme?
Toxoplasma inficerer nerveceller. Visse versioner af ALOX12 og NALP1 kan hjælpe en smittet person med at etablere et stærkt, tidligt, beskyttende immunforsvar, der dræber parasitter, inficerede celler og celler i nærheden. Men vi ved også, at ALOX12 er forbundet med sygdomme i forbindelse med aldring og hukommelsestab. Da vi anvendte vores resultater om ALOX12 i forbindelse med systembiologiske programmer, der bruges til at kortlægge veje, indså vi, at mange af disse veje også var i spil i forskellige neurodegenerative sygdomme såsom Alzheimers og endda skizofreni. Nogle kan også bidrage til åreforkalkning eller diabetes. Når dette kraftige immunforsvar forbliver på arbejdspladsen, kan det have virkninger, der kan være skadelige. mere effektive lægemidler eller en vaccine kunne beskytte mod de ødelæggende sygdomme, som denne parasit forårsager. Dette nylige arbejde rejser muligheden for, at bedre behandlinger, ved hurtigt at kontrollere eller eliminere infektionen, også kan reducere de aldersrelaterede sygdomme, som vi spekulerer på kan forbindes med toxoplasma for nogle mennesker.
Dette er et stort projekt. Det ser ud til, at du har mange partnere i denne indsats, ikke?
Det har været et vidunderligt samarbejde med kolleger i Frankrig, England og Canada og et hold på University of Kansas, sammen med arbejdet fra en bemærkelsesværdig gruppe unge forskere i mit eget laboratorium.

Det er opmuntrende. Hvem arbejder du sammen med for at komme videre med denne opdagelse?
Vi arbejder i vores egne forskningsprogrammer og laboratoriegruppe og med kolleger i New Haven, J Craig Ventner Institute og Institute for Systems Biology i Seattle og en række andre kolleger. Vi er meget begejstrede for den indsigt og det potentiale for at fremme forebyggelse og behandling, som dette arbejde giver.