Immunogenität, definiert als die Fähigkeit einer Substanz, eine Immunantwort hervorzurufen, ist der Schlüssel zu einem erfolgreichen und sicheren biopharmazeutischen Arzneimittelentwicklungsprogramm. Therapeutische Antikörper, Enzymtherapien, Peptide und Kombinationsprodukte können eine Immunreaktion hervorrufen, die sich auf ihre Sicherheit und Wirksamkeit auswirken kann.
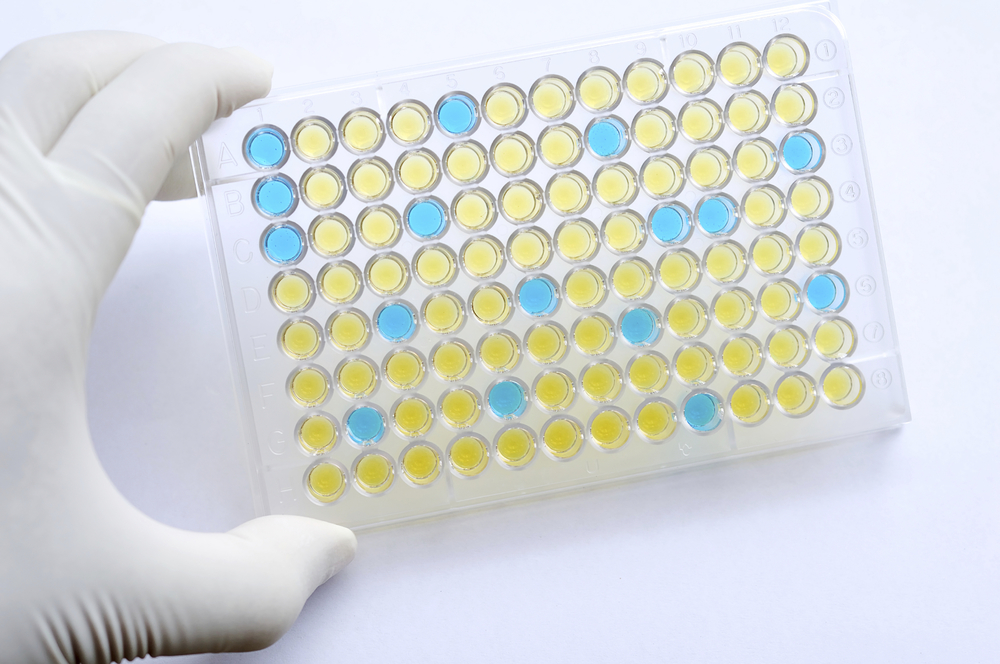 Beispiel für eine ELISA-Testplatte
Beispiel für eine ELISA-Testplatte
Wie Biologika eine Immunreaktion hervorrufen
Viele Arten von Substanzen, die dem menschlichen Körper verabreicht werden, können eine Immunreaktion hervorrufen. Biotherapeutika können jedoch besonders immunogen sein, weil die Größe dieser Moleküle dem Körper vorgaukeln kann, dass es sich um fremde Eindringlinge handelt, was das Immunsystem zum Handeln veranlasst. Diese großen Moleküle können auch denaturieren, wodurch sich ihr Profil verändert, oder sie können aggregieren, wodurch noch größere Partikel entstehen. Letztlich können diese Eigenschaften das Immunogenitätsprofil eines Biotherapeutikums verändern oder verstärken.
Es wurden neue Technologien entwickelt – zum Beispiel die PEGylierung -, um die immunologische Wirkung von Biotherapeutika zu verringern. Die Wirksamkeit dieser Versuche, die Immunogenität zu verringern, ist jedoch unterschiedlich. Aus diesem Grund ist die Prüfung der Immunogenität eines in der Entwicklung befindlichen Produkts so wichtig. Darüber hinaus sind Immunogenitätstests auch in einem Entwicklungsprogramm für Biosimilars notwendig. Dies liegt daran, dass die kleinen Änderungen in der Herstellung von Biotherapeutika große Veränderungen in ihrem Immunogenitätsprofil bewirken können. Daher müssen Biosimilars, die fast ausnahmslos unter anderen Bedingungen als ihre biologischen Ausgangsstoffe hergestellt werden, weiterhin auf ihre Immunogenität getestet werden.
Was sind Immunogenitätstests
Immunogenitätstests bieten eine Möglichkeit, die potenziellen Immunreaktionen von Biologika und Biosimilars zu messen. Häufig ist für ein einzelnes Biologikum eine Reihe von Tests erforderlich, um ein umfassendes Bild der potenziellen Immunogenität zu erhalten. Die FDA schreibt vor, dass die Tests so konzipiert sein sollten, dass sie eine ausreichende Empfindlichkeit bieten, frei von störenden Interferenzen sind, physiologische Folgen erkennen können und potenzielle Risiken auf der Grundlage des Profils des Therapeutikums und der Zielpatientenpopulation berücksichtigen.
Durch die Entwicklung von Tests unter Berücksichtigung dieser Faktoren ist es möglich, prädiktive Daten über die Stärke und die Art der Immunreaktion zu sammeln, die ein Arzneimittel beim Menschen hervorrufen kann.
Arten der Immunogenitätsanalyse
Für einige Biologika ist ein Gesamtantikörpertest (zur Messung der Antikörper, die Teil der Immunreaktion sind), der Screening-, Bestätigungs- und Titer-Komponenten umfasst, ausreichend, um ein Immunogenitätsprofil zu erstellen. In anderen Fällen kann ein neutralisierender Antikörper-Assay oder ein zellbasierter Bioassay notwendig und aussagekräftig sein. ELISA (enzyme-linked immunosorbent assay) ist ebenfalls eine nützliche Methode zum Nachweis von Antikörper-Antigen-Komplexen.
Darüber hinaus kann das Aggregationspotenzial eines Biotherapeutikums mit Hilfe von Größenausschlusschromatographie und HPLC in Kombination mit Laser-Lichtstreuung gemessen werden. Dies kann dazu beitragen, ein umfassenderes Bild des gesamten immunogenen Profils eines Wirkstoffs zu erhalten.
Das Ziel all dieser Tests ist letztlich die Vorhersage der klinischen Wirkung der Immunreaktionen von Patienten auf Biotherapeutika. Die Immunogenität spielt bei der Arzneimittelentwicklung eine wichtige Rolle. Daher ist ein gut durchdachtes und gut ausgeführtes Programm der Schlüssel zur Herstellung sicherer und wirksamer biologischer Therapien.
Um mehr über die Immunogenitätstests von Pacific BioLabs zu erfahren, besuchen Sie die Seite Immunogenitätstests von PBL.
Quellen
Nachrichten aus der Gentechnik und Biotechnologie: Vorgeschlagene Standards für Immunogenitätstests – http://www.genengnews.com/gen-articles/proposed-standards-for-immunogenicity-testing/4145/
FDA: Immunogenicity of Protein-Based Therapeutics – http://www.fda.gov/BiologicsBloodVaccines/ScienceResearch/BiologicsResearchAreas/ucm246804.htm
Wikipedia: Immunogenität – http://en.wikipedia.org/wiki/Immunogenicity